Trộn 100ml dung dịch Ba(OH)2 0,06M với 400ml dung dịch HCl 0,02M. Tính pH của dung dịch tạo thành
K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Những câu hỏi liên quan

14 tháng 10 2017
Đáp án B
nOH-= 0,03 mol; nBa2+ = 0,01 mol
nH+ = 0,035 mol; nSO4(2-) = 0,015 mol
H+ + OH- → H2O
0,035 0,03
nH+ dư = 5.10-3 mol; [H+] dư = 5.10-3/0,5 = 0,01 suy ra pH = 2

13 tháng 7 2018
Đáp án A
nHNO3 = 0,3 mol; nBa(OH)2 = 0,05 mol
H++ OH- → H2O
0,3 0,1
nH+ dư = 0,2 mol nên [H+]dư = nH+/ Vdd = 0,2/0,25 = 0,8 M suy ra pH = 0,097

HP
7 tháng 10 2021
a, \(n_{OH^-}=0,2.0,1+0,1.2.0,4=0,1\left(mol\right)\)
\(\Rightarrow\left[OH^-\right]=\dfrac{0,1}{0,5}=0,2M\)
\(\Rightarrow\left[H^+\right]=5.10^{-14}M\)
\(\Rightarrow pH\approx13,3\)
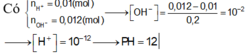

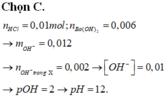
Ta có: \(\left\{{}\begin{matrix}n_{Ba\left(OH\right)_2}=0,1.0,06=0,006\left(mol\right)\\n_{HCl}=0,4.0,02=0,008\left(mol\right)\end{matrix}\right.\)
PTHH: `Ba(OH)_2 + 2HCl -> BaCl_2 + 2H_2O`
0,006------->0,003
`=>` \(\left[H^+\right]=C_{M\left(HCl\right)}=\dfrac{0,008-0,003}{0,1+0,4}=0,01M=10^{-2}M\)
`=> pH = 2`