Cho 10,8 gam Al vào 200 gam dd HCl 29,2% , thu được dd X . Tính nồng độ phàn trăm các chất tan dd X
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


HD: em tính số mol Al = 0,4 mol và số mol HCl = 1,6 mol
Viết PTHH
Từ tỉ lệ mol: nAl/nHCl theo PTHH = 1/3 >0,4/1,6 nên Al hết và dd HCl dư
+ Dung dịch X sau Phản ứng gồm: AlCl3 tạo thành và HCl dư
+ Khối lượng dung dịch sau phản ứng = khối lượng Al + khối lượng đ HCl ban đầu - khối lượng H2
+ Áp dụng CT tính C% tính C% của AlCl3 và C% của HCl dư

a) Gọi số mol Zn, Al là a,b (mol)
=> 65a + 27b = 9,2 (1)
\(n_{H_2}=\dfrac{0,5}{2}=0,25\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
a---->2a-------------->a
2Al + 6HCl --> 2AlCl3 + 3H2
b----->3b--------------->1,5b
=> a + 1,5b = 0,25 (2)
(1)(2) => a = 0,1 (mol); b = 0,1 (mol)
=> \(\left\{{}\begin{matrix}\%m_{Zn}=\dfrac{0,1.65}{9,2}.100\%=70,65\%\\\%m_{Al}=\dfrac{0,1.27}{9,2}.100\%=29,35\%\end{matrix}\right.\)
b) nHCl = 2a + 3b = 0,5 (mol)
=> \(C\%_{dd.HCl}=\dfrac{0,5.36,5}{200}.100\%=9,125\%\)

a, \(Cu+2H_2SO_{4\left(đ\right)}\underrightarrow{t^o}CuSO_4+SO_2+2H_2O\)
b, \(n_{SO_2}=\dfrac{3,7185}{24,79}=0,15\left(mol\right)\)
Theo PT: \(n_{Cu}=n_{CuSO_4}=n_{SO_2}=0,15\left(mol\right)\)
\(\Rightarrow m_{Cu}=0,15.64=9,6\left(g\right)=m\)
Theo PT: \(n_{H_2SO_4}=2n_{SO_2}=0,3\left(mol\right)\Rightarrow C\%_{H_2SO_4}=\dfrac{0,3.98}{200}.100\%=14,7\%=x\)
Ta có: m dd sau pư = 9,6 + 200 - 0,15.64 = 200 (g)
\(\Rightarrow C\%_{CuSO_4}=\dfrac{0,15.160}{200}.100\%=12\%\)

mH2SO4= \(\dfrac{300.7,35}{100}=22,05g\)
nH2SO4= \(\dfrac{22,05}{98}=0,225 mol\)
mHCl= \(\dfrac{200.7,3}{100}=14,6g\)
nHCl= \(\dfrac{14,6}{36,5}=0,4mol\)
H2SO4 + 2HCl → 2H2O + Cl2 ↑+ SO2 ↑
n trước pư 0,225 0,4
n pư 0,2 ← 0,4 → 0,4 → 0,2 → 0,2 mol
n sau pư dư 0,025 hết
a) mCl2= 0,2. 71= 14,2g
mSO2= 64. 0,2= 12,8g
mH2O= 18. 0,4=7,2g
mdd sau pư= 300 +200 -14,2 -12,8= 473g
C%dd H2O= \(\dfrac{7,2.100}{473}=1,52\)%
b) Mg + 2H2O → Mg(OH)2 + H2 ↑
x → 2x → x → x
Fe + 2H2O → Fe(OH)2 + H2↑
y → 2y → y → y
Gọi x,y lần lượt là số mol của Mg,Fe.
Ta có hệ phương trình:
24x + 56y = 8,7 x= \(\dfrac{5}{64}\)
⇒
2x + 2y = 0,4 y= \(\dfrac{39}{320}\)
VH2= 22,4. \((\dfrac{5}{64}+\dfrac{39}{320})\)= 4,48l
mhh MG(OH)2, Fe(OH)2= 8,7 +250 - 2.(\(\dfrac{5}{64}+\dfrac{39}{320}\)) = 2258,3g
mMg=24. \(\dfrac{5}{64}\)=1.875g
mFe= 8,7-1,875= 6,825g

Ta có: \(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
Ta lại có: \(C_{\%_{H_2SO_4}}=\dfrac{m_{H_2SO_4}}{294}.100\%=20\%\)
=> \(m_{H_2SO_4}=58,8\left(g\right)\)
=> \(n_{H_2SO_4}=\dfrac{58,8}{98}=0,6\left(mol\right)\)
PTHH: 2Al + 3H2SO4 ---> Al2(SO4)3 + 3H2
Ta thấy: \(\dfrac{0,2}{1}=\dfrac{0,6}{3}\)
Vậy không có chất dư.
Theo PT: \(n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{2}.n_{Al}=\dfrac{1}{2}.0,2=0,1\left(mol\right)\)
=> \(m_{Al_2\left(SO_4\right)_3}=0,1.342=34,2\left(g\right)\)
Ta có: \(m_{dd_{Al_2\left(SO_4\right)_3}}=294+5,4-\left(\dfrac{3}{2}.0,2.2\right)=298,8\left(g\right)\)
=> \(C_{\%_{Al_2\left(SO_4\right)_3}}=\dfrac{34,2}{298,8}.100\%=11,45\%\)

a, \(Fe+2HCl\rightarrow FeCl_2+H_2\)
Ta có: \(n_{Fe}=\dfrac{14}{56}=0,25\left(mol\right)\)
Theo PT: \(\left\{{}\begin{matrix}n_{HCl}=2n_{Fe}=0,5\left(mol\right)\\n_{H_2}=n_{Fe}=0,25\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow V_{H_2}=0,25.24,79=6,1975\left(l\right)\)
\(a=C_{M_{HCl}}=\dfrac{0,5}{0,1}=5\left(M\right)\)
b, Theo PT: \(n_{FeCl_2}=n_{Fe}=0,25\left(mol\right)\)
Ta có: \(n_{AgNO_3}=0,4.1,3=0,52\left(mol\right)\)
PT: \(2AgNO_3+FeCl_2\rightarrow Fe\left(NO_3\right)_2+2AgCl_{\downarrow}\)
______0,5______0,25______0,25________0,5 (mol)
\(AgNO_3+Fe\left(NO_3\right)_2\rightarrow Fe\left(NO_3\right)_3+Ag_{\downarrow}\)
0,02______0,02________0,02________0,02 (mol)
⇒ m = mAgCl + mAg = 0,5.143,5 + 0,02.108 = 73,91 (g)
- Dd sau pư gồm: Fe(NO3)3: 0,02 (mol) và Fe(NO3)2: 0,25 - 0,02 = 0,23 (mol)
\(\Rightarrow\left\{{}\begin{matrix}C_{M_{Fe\left(NO_3\right)_3}}=\dfrac{0,02}{0,1+0,4}=0,04\left(M\right)\\C_{M_{Fe\left(NO_3\right)_2}}=\dfrac{0,23}{0,1+0,4}=0,46\left(M\right)\end{matrix}\right.\)
\(Fe+2HCl->FeCl_2+H_2\\ a.V=\dfrac{14}{56}\cdot22,4=5,6\left(L\right)\\ a=\dfrac{\dfrac{14}{56}\cdot2}{0,1}=5\left(M\right)\\ b.n_{AgNO_3}=0,4\cdot1,3=0,52mol\\ FeCl_2+AgNO_3->Fe\left(NO_3\right)_2+AgCl\\ Fe\left(NO_3\right)_2+AgNO_3->Ag+Fe\left(NO_3\right)_3\\ m=0,25\cdot143,5+0,25\cdot108=62,875\left(g\right)\\ C_{M\left(AgNO_3\right)}=\dfrac{0,02}{0,5}=0,04M\\ C_{M\left(Fe\left(NO_3\right)_3\right)}=\dfrac{0,25}{0,5}=0,5M\)

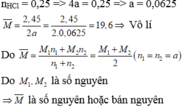
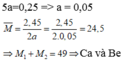

Ta có: \(\left\{{}\begin{matrix}n_{Al}=\dfrac{10,8}{27}=0,4\left(mol\right)\\n_{HCl}=\dfrac{200.29,2\%}{36,5}=1,6\left(mol\right)\end{matrix}\right.\)
PTHH: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
ban đầu 0,4 1,6
phản ứng 0,4---->1,2
sau phản ứng 0 0,4 0,4 0,6
`=>` \(m_{ddX}=10,8+200-0,6.2=209,6\left(g\right)\)
`=>` \(\left\{{}\begin{matrix}C\%_{AlCl_3}=\dfrac{0,4.133,5}{209,6}.100\%=25,48\%\\C\%_{HCl}=\dfrac{0,4.36,5}{209,6}.100\%=6,97\%\end{matrix}\right.\)