Lấy 2 ml dung dịch acid H2SO4 đậm đặc 97% (D= 1,83 g/mL) pha loãng với nước cất
bằng bình định mức 500 ml. Tính nồng độ mole và nồng đương lượng của dung dịch sau
khi pha loãng?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đổi: 40ml = 0,04l
160ml = 0,16l
nH2SO4 = 0,04 . 8 = 0,32 (mol)
CMddH2SO4 (sau khi pha loãng) = 0,32/0,16 = 2M

\(H_2SO_4+Na_2CO_3\rightarrow Na_2SO_4+CO_2+H_2O\)
\(n_{H_2SO_4}=n_{Na_2CO_3}=0,024.0,1=0,0024\left(mol\right)\)
=> \(CM_{H_2SO_4\left(bđ\right)}=\dfrac{0,0024}{0,002}=1,2M\)

Thể tích nước cần dùng để pha loãng.
Khối lượng của 100ml dung dịch axit 98%
100ml × 1,84 g/ml = 184g
Khối lượng H2SO4 nguyên chất trong 100ml dung dịch trên: 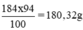
Khối lượng dung dịch axit 20% có chứa 180,32g H2SO4 nguyên chất: 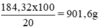
Khối lượng nước cần bổ sung vào 100ml dung dịch H2SO4 98% để có được dung dịch 20%: 901,6g – 184g = 717,6g
Vì D của nước là 1 g/ml nên thể tích nước cần bổ sung là 717,6 ml.


\(m_{ddH_2SO_4}=2.1,83=3,66\left(g\right)\\ n_{H_2SO_4}=\dfrac{3,66.97\%}{98}\left(mol\right)\\ C_{MddH_2SO_4\left(sau.pha\right)}=\dfrac{\dfrac{3,66.97\%}{98}}{0,5}\approx0,072453\left(M\right)\\ C_{NddH_2SO_4}=\dfrac{3,66.97\%}{49.500}.100=0,0145\left(N\right)\)
cho em hỏi Cn h2so4 em tính bằng Cm h2so4 * 2 được không ạ ?