Tính số phân tử nước, số nguyên tử H và O trong 9 gam phân tử nước tinh khiết.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


B
Khối lượng 1 phân tử nước m 0 = 2 . 1 , 67 . 10 - 27 + 26 , 56 . 10 - 27 = 29 , 9 . 10 - 27 kg
Số phân tử nước trong 1 gam nước
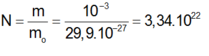

Số phân tử nước: 3.6,022.1023= 18,066.1023 (phân tử)
Số nguyên tử H: 2. 18,066.1023= 36,132. 1023 (ng.tử)
Số nguyên tử O = Số phân tử nước: 18,066.1023 (ng.tử)

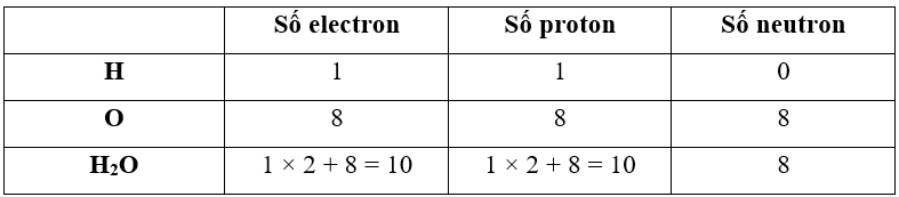
- Số electron dùng chung của nguyên tử H và O là 4
- Trong phân tử nước:
+ Nguyên tử O có 8 electron lớp ngoài cùng => Giống khí hiếm Ne
+ Nguyên tử H có 2 electron lớp ngoài cùng => Giống khí hiếm He

MH2O=1.2+16=18(g)
Vậy 0,05g nước chứa số mol là: nH2O=\(\dfrac{0,05}{18}\)=2,77.10−3mol
Trong 1 mol H2O chứa 6,02.1023 phân tử nước
→ 2,77.10-3mol H2O chứa x phân tử nước
Vậy x=\(\dfrac{2,77.10^{-3}.6,02.10^{23}}{1}\)=1,667.1021
nH2O = 0,05 : 18 = 1/360 (mol)
=> số phân tử của nước là : 1/360 . 6.1023= 0,167.1023

\(n_{SO_3}=\dfrac{2}{80}=0,025\left(mol\right)\\ V_{SO_3}=0,025.22,4=0,56\left(l\right)\\ m_S=0,025.32=0,8\left(g\right)\\ m_O=0,025.48=1,2\left(g\right)\\ 1nguyêntửS,3nguyêntửO\)

a/ 1 mol
b/ n = \(\frac{6,022.10^{23}}{6,022.10^{23}}=1\) (mol)
c/ \(n=\frac{6,022.10^{23}}{6,022.10^{23}}=1\) (mol)


\(n_{H_2O}=\dfrac{9}{18}=0.5\left(mol\right)\)
Số phân tử H2O : \(0.5\cdot6\cdot10^{23}=3\cdot10^{23}\left(pt\right)\)
Số nguyên tử H : \(0.5\cdot2\cdot6\cdot10^{23}=6\cdot10^{23}\left(nt\right)\)
Số nguyên tử O : \(0.5\cdot6\cdot10^{23}=3\cdot10^{23}\left(nt\right)\)
n H2O=\(\dfrac{9}{18}=0,5mol\)
số nguyên tử H là :0,5.2.6,02.1023=6.02.1023 pt
số nguyên tử O là :0,5.6,02.1023=3,01.1023 pt