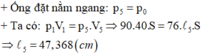Một xylanh đươc nằm ngang, lúc đầu piston cách nhiệt và cách đều 2 đầu xylanh 1 khoảng l = 50cm và không khí chứa trong xylanh có nhiệt độ 27°C áp suất 1atm. Sau đó không khí ở đầu bên trái được nung nóng lên 67°C thì piston sẽ di chuyển 1 đoạn x, tìm giá trị của x.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án: A
Ta có:
- Trạng thái 1: T 1 = 27 + 273 = 300 K p 1 = 1 a t m V 1 = n V = 1000.4 = 4000 l
- Trạng thái 2: T 2 = 42 + 273 = 315 K p 2 = ? V 2 = 2 m 3 = 2000 l
Áp dụng phương trình trạng thái của khí lý tưởng, ta có:
p 1 V 1 T 1 = p 2 V 2 T 2 ⇒ p 2 = p 1 V 1 T 2 T 1 V 2 = 1.4000.315 300.2000 = 2,1 a t m

Chọn D.
Gọi p 1 , V 1 và p 2 , V 2 là các áp suất, thể tích của cột không khí trong ống tương ứng với miệng ống ở phía trên và ống nằm ngang.
Ống thẳng đứng, miệng ở phía trên:
p 1 = p 0 = p H g = (76 + 15) cmHg = 91 cmHg;
Thể tích của cột không khí: V 1 = l 1 .S
Khi ống nằm ngang cột thủy ngân không có tác dụng lên cột không khí nên:
p 2 = p a = 76cmHg
Khối khí trong ống không đổi và nhiệt độ không đổi nên theo định luật Bôi-lơ – Ma-ri-ốt:
p 1 V 1 = p 2 V 2
↔ V 2 / V 1 = p 1 / p 2 = 91/76
→ l 2 / l 1 = 91/76 → l 2 = 35,9 cm

Chọn D.
Gọi p 1 , V 1 và p 2 , V 2 là các áp suất, thể tích của cột không khí trong ống tương ứng với miệng ống ở phía trên và ống nằm ngang.
Ống thẳng đứng, miệng ở phía trên:
p 1 = p 0 + p H g = (76 + 15) cmHg = 91 cmHg;
Thể tích của cột không khí: V 1 = l 1 S
Khi ống nằm ngang cột thủy ngân không có tác dụng lên cột không khí nên:
p 2 = p a = 76cmHg
Khối khí trong ống không đổi và nhiệt độ không đổi nên theo định luật Bôi-lơ – Ma-ri-ốt:
p 1 V 1 = p 2 V 2
↔ V 2 / V 1 = p 1 / p 2 = 91/76
→ l 2 / l 1 = 91/76 → l 2 = 35,9 cm

Trạng thái 1: \(\left\{{}\begin{matrix}p_1=2\cdot10^5Pa\\T_1=27^oC=300K\end{matrix}\right.\)
Trạng thái 2: \(\left\{{}\begin{matrix}p_2=???\\T_2=627^oC=900K\end{matrix}\right.\)
Quá trình đẳng tích:
\(\dfrac{p_1}{T_1}=\dfrac{p_2}{T_2}\Rightarrow\dfrac{2\cdot10^5}{300}=\dfrac{p_2}{900}\)
\(\Rightarrow p_2=6\cdot10^5Pa\)

Chọn D.
Gọi và là các áp suất, thể tích của cột không khí trong ống tương ứng với miệng ống ở phía trên và ống nằm ngang.
Ống thẳng đứng, miệng ở phía trên: p1 = p0 + pHg = (76 + 15) cmHg = 91 cmHg;
Thể tích của cột không khí: V1 = ℓ1.S
Khi ống nằm ngang cột thủy ngân không có tác dụng lên cột không khí nên:
p2 = pa = 76cmHg
Khối khí trong ống không đổi và nhiệt độ không đổi nên theo định luật Bôi-lơ – Ma-ri-ốt: p1 .V1 = p2.V2 ↔ V2/V1 = p1/p2 = 91/76 → ℓ2/ℓ1 = 91/76 → ℓ2 = 35,9 cm

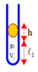
a) Ống đặt thẳng đứng, miệng ở dưới:
Gọi p 1 , V 1 và p 2 , V 2 là các áp suất, thể tích của cột không khí trong ống tương ứng với miệng ống ở phía trên và phía dưới. Ta có:
p 1 = p o + h = 76 + 15 = 91 c m H g ;
V 1 = l 1 S = 30 S
p 2 = p o − h = 76 − 15 = 61 c m H g ;
V 1 = l 2 S
Khối khí trong ống không đổi và nhiệt độ không đổi nên theo định luật Bôi-lơ – Ma-ri-ốt:
p 1 V 1 = p 2 V 2 ⇔ 91.30 S = 61 l 2 S
⇒ l 2 = 44 , 75 c m .
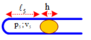
b) Ống đặt nằm ngang:
Cột thủy ngân không có tác dụng lên cột không khí nên:
p 3 = p o .
Theo định luật Bôi-lơ – Ma-ri-ốt ta có:
p 1 V 1 = p 3 V 3 ⇔ 91.30 S = 76 l 3 S
⇒ l 3 = 35 , 9 c m