Câu 1: Viết PT dạng phân tử và ion rút gọn của các PƯ trong dd theo sơ đồ sau:
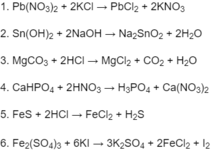
a) \(Pb\left(NO3\right)_2\) + ? → \(PbCl_2\downarrow\) + ?
b) \(\left(NH_4\right)_2CO_3\) + ? → ? + \(NH_3\uparrow\) + \(H_2O\)
Câu 2: Pha 80 ml dd \(Ba\left(OH\right)_2\) 0,25M với 20 ml dd hỗn hợp \(HNO_3\) 0,5M và \(H_2SO_4\) 0,5M, thu được dd A.
a) Tìm nồng độ mol ion của dung dịch A (bỏ qua sự điện li của nước)?
b) Tìm \(pH\) dung dịch A?

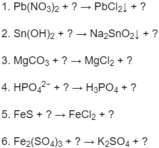
Câu 1:
a) \(Pb\left(NO_3\right)_2+CaCl_2\rightarrow PbCl_2\downarrow+Ca\left(NO_3\right)_2\)
\(Pb^{2+}+2Cl^-\rightarrow PbCl_2\downarrow\)
b) \(\left(NH_4\right)_2CO_3+2KOH\rightarrow K_2CO_3+2NH_3\uparrow+H_2O\)
\(NH_4^++OH^-\rightarrow NH_3\uparrow+H_2O\)
Câu 2:
a) Ta có:
\(\left\{{}\begin{matrix}n_{OH^-}=2n_{Ba\left(OH\right)_2}=0,08.0,25.2=0,04\left(mol\right)\\n_{H^+}=n_{HNO_3}+2n_{H_2SO_4}=0,5.0,02+0,02.0,5.2=0,03\left(mol\right)\end{matrix}\right.\)
\(\left\{{}\begin{matrix}n_{Ba^{2+}}=n_{Ba\left(OH\right)_2}=0,08.0,25=0,02\left(mol\right)\\n_{SO_4^{2-}}=0,02.0,5=0,01\left(mol\right)\end{matrix}\right.\)
PTHH: \(H^++OH^-\rightarrow H_2O\)
0,03--->0,03
\(Ba^{2+}+SO_4^{2-}\rightarrow BaSO_4\downarrow\)
0,01<---0,01
`=>` \(ddA:\left\{{}\begin{matrix}n_{OH^-\left(dư\right)}=0,04-0,03=0,01\left(mol\right)\\n_{Ba^{2+}\left(dư\right)}=0,02-0,01=0,01\left(mol\right)\\n_{NO_3^-}=n_{HNO_3}=0,02.0,5=0,01\left(mol\right)\end{matrix}\right.\)
Ta có: \(V_{ddA}=0,08+0,02=0,1\left(l\right)\)
`=>` \(\left[OH^-\right]=\left[Ba^{2+}\right]=\left[NO_3^-\right]=\dfrac{0,01}{0,1}=0,1M\)
b) \(pOH=-\text{log}\left(0,1\right)=1\)
`=>` \(pH=14-1=13\)