Nhỏ từ từ từng giọt đến hết 100ml dd hỗn hợp Na2CO3 0,1M và KHCO3 0,2M vào 350ml dd HCl 0,1 và khuấy đều. Sau phản ứng, thu được V ml khí CO2 (đktc). Tính V?
K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Những câu hỏi liên quan

14 tháng 9 2018
Đáp án C
Ta có: n H + = 0,125. 0,1= 0,0125 mol
CO32- + 2H+ → CO2 + H2O
0,005 0,01 0,005
HCO3- + H+ → CO2 + H2O
0,0075 0,0075 0,0075
Nếu phản ứng xảy ra vừa đủ thì :
0,0175 mol H+ → 0,0125 mol CO2
Theo bài ra axit thiếu
⇒ 0,0125 mol H+ → 1/112 mol CO2
⇒ V = 0,2 lít = 200 ml
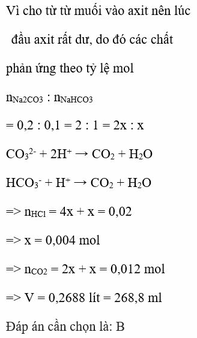


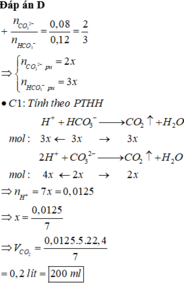

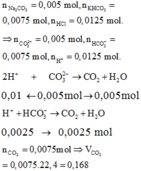
\(n_{Na_2CO_3}=0,01\left(mol\right)\)
\(n_{K_2CO_3}=0,02\left(mol\right)\)
\(Na_2CO_3+2HCl\rightarrow2NaCl+H_2O+CO_2\)
0,01 → 0,01
\(KHCO_3+HCl\rightarrow KCl+H_2O+CO_2\)
0,02 → 0,02
\(\Rightarrow\Sigma V_{CO_2}=\left(0,01+0,02\right)22,4=0,672\left(l\right)\)
Bạn xem lại nhé \(n_{HCl\left(bđ\right)}=0,35.0,1=0,035\left(mol\right)\)
Mà \(n_{HCl\left(pư\right)}=2n_{Na_2CO_3}+n_{KHCO_3}=0,01.2+0,02=0,04\left(mol\right)>0,035\)
Vậy muối dư, HCl hết