Cho 4.48 lít khí H2 đi qua 48 gam fe2o3 nung nóng thu được chất rắn X a) Tính khối lượng của X. b) Tính khối lượng dd HCl 3.65% vừa đủ để tác dụng với chất rắn X. c) Tính nồng độ phần trăm của các chất có trong dd thu được sau phản ứng.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

dẫn luồng khí CO đi qua ống sứ chứa 0,3 mol hỗn hợp A(FeO và Fe2O3) nung nóng . Sau một thời gian phản ứng thu được 24 gam chất rắn B gồm FeO,Fe3O4,Fe2O3,Fe và

Chọn đáp án C
Sơ đồ quá trình phản ứng:
C + H2O → hh X = {H2; CO; CO2} || X + a mol Fe3O4; b mol CuO → 25,92 gam hh Y.
(2a + 0,5b) mol H2 + hh Y → {Fe; Cu} + H2O.
Gọi số mol {CO; H2} trong X là z mol → cần đúng z mol O trong oxit đề → {CO2; H2O}.
→ 160a + 80b = 25,92 + 16z (1). Lại có để chuyển hết (3a + b) mol O trong oxit → {CO2; H2O}
thì cần vừa đủ z + 2a + 0,5b mol hh {CO; H2} → 3a + b = z + 2a + 0,5b ↔ a + 0,5b = z (2).
Từ (1) và (2) ta có z = 0,18 mol. Đến đây có 2 hướng xử lí:
ᴥ cách 1: thường các bạn sẽ tìm mối ràng buộc nữa thì C + H2O → CO + H2 || C + 2H2O → CO2 + 2H2.
Bằng cách gọi số mol C ở các pt lần lượt là x, y mol → 2x + 3y = 0,2 mol
và 2x + 2y = nhh CO + H2 0,18 mol. Giải tìm ra đáp án C. ♣.
Theo hướng này có thể nhanh hơn như sau: nCO2 = 0,2 - z = 0,02 mol.
Thay vào 2 phương trình trên cũng ra kết quả tương tự.
ᴥ cách 2: có thể đi theo hướng sau: hiểu rõ vấn đề + rút gọn suy nghĩ, cần hình dung:
C + H2O →....→.... cuối cùng sẽ thu được CO2 + H2O.
như vậy 0,18 mol O là ở trong CO2 luôn → có 0,09 mol C.
→ trong Y có 0,09 mol CO và CO2 (bảo toàn C) → có 0,11 mol H2O
→ mY = 0,09 × 44 + 0,11 × 18 - 0,18 × 16 = 3,06 gam. → dY/H2 = 3,06 ÷ 0,2 ÷ 2 = 7,65.
Chọn đáp án C. ♣
p/s: bài toán này khai thác điểm đặc biệt Fe2O3 và CuO có M = 160 và 80 + bản chất CO và H2 cùng nhận 1 O.

Đáp án D
Sơ đồ quá trình phản ứng:
C + H2O → hh X = {H2; CO; CO2} || X + a mol Fe3O4; b mol CuO → 25,92 gam hh Y.
(2a + 0,5b) mol H2 + hh Y → {Fe; Cu} + H2O.
Gọi số mol {CO; H2} trong X là z mol → cần đúng z mol O trong oxit đề → {CO2; H2O}.
→ 160a + 80b = 25,92 + 16z (1). Lại có để chuyển hết (3a + b) mol O trong oxit → {CO2; H2O}
thì cần vừa đủ z + 2a + 0,5b mol hh {CO; H2} → 3a + b = z + 2a + 0,5b ↔ a + 0,5b = z (2).
Từ (1) và (2) ta có z = 0,18 mol. Đến đây có 2 hướng xử lí:
cách 1: thường các bạn sẽ tìm mối ràng buộc nữa thì C + H2O → CO + H2 || C + 2H2O → CO2 + 2H2.
Bằng cách gọi số mol C ở các pt lần lượt là x, y mol → 2x + 3y = 0,2 mol
và 2x + 2y = nhh CO + H2 0,18 mol. Giải tìm ra đáp án C. ♣.
Theo hướng này có thể nhanh hơn như sau: nCO2 = 0,2 - z = 0,02 mol.
Thay vào 2 phương trình trên cũng ra kết quả tương tự.
cách 2: có thể đi theo hướng sau: hiểu rõ vấn đề + rút gọn suy nghĩ, cần hình dung:
C + H2O →....→.... cuối cùng sẽ thu được CO2 + H2O.
như vậy 0,18 mol O là ở trong CO2 luôn → có 0,09 mol C.
→ trong Y có 0,09 mol CO và CO2 (bảo toàn C) → có 0,11 mol H2O
→ mY = 0,09 × 44 + 0,11 × 18 - 0,18 × 16 = 3,06 gam. → dY/H2 = 3,06 ÷ 0,2 ÷ 2 = 7,65.
Chọn đáp án C.
p/s: bài toán này khai thác điểm đặc biệt Fe2O3 và CuO có M = 160 và 80 + bản chất CO và H2 cùng nhận 1 O.

Gọi $n_{Fe_2O_3} = a(mol) ; n_{Fe} = b(mol)$
$\Rightarrow 160a + 56b = 12(1)$
$Fe_2O_3 + 3H_2 \xrightarrow{t^o} 2Fe + 3H_2O$
Suy ra : $2a.56 + 56b = 10,08(2)$
Từ (1)(2) suy ra a = 0,04 ; b = 0,1
$\Rightarrow m_{Fe_2O_3} = 0,04.160 = 6,4(gam); m_{Fe} = 0,1.56 = 5,6(gam)$
TN1 Fe ---> Fe
x x mol
FeO+ H2 ---> Fe + H2O
y y
Fe2O3 + 3H2---> 2Fe + 3H2O
z 2z
=> 56x + 72y+ 160z=2,36
TN2 Fe + CuSO4---> FeSO4+ Cu
x x mol
FeO và Fe2O3 không tác dụng
=> 64x+ 72y+ 16O z=2,48
lại có 56x+ 72y+ 160z=2,36
giả hệ 3 pt => x=0,015 ,y= 0,01 , z=0,005
=> mFe=0,84 gan , mFeO=0,72 gam, mFe2O3=0,8 gam.

Đáp án B
Phản ứng tổng quát : CO + Ooxit -> CO2
=> mrắn giảm = mO pứ = 0,8g => nO pứ = nCO2 = 0,05 mol
=> X gồm 0,05 mol CO và 0,05 mol CO2
=> dX/H2 = 18

Đáp án B
Phản ứng tổng quát : CO + Ooxit -> CO2
=> mrắn giảm = mO pứ = 0,8g => nO pứ = nCO2 = 0,05 mol
=> X gồm 0,05 mol CO và 0,05 mol CO2
=> dX/H2 = 18

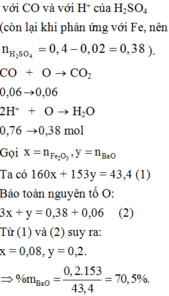
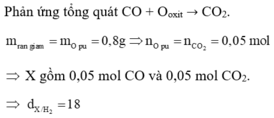
a) \(\left\{{}\begin{matrix}n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\n_{Fe_2O_3}=\dfrac{48}{160}=0,3\left(mol\right)\end{matrix}\right.\)
PTHH: \(Fe_2O_3+3H_2\xrightarrow[]{t^o}2Fe+3H_2O\)
Xét tỉ lệ: \(0,3>\dfrac{0,2}{3}\Rightarrow Fe_2O_3\) dư
Theo PT: \(\left\{{}\begin{matrix}n_{Fe_2O_3\left(pư\right)}=\dfrac{1}{3}n_{H_2}=\dfrac{1}{15}\left(mol\right)\\n_{Fe}=\dfrac{2}{3}n_{H_2}=\dfrac{2}{15}\left(mol\right)\end{matrix}\right.\)
`=>` \(m_X=\left(0,3-\dfrac{1}{15}\right).160+\dfrac{2}{15}.56=44,8\left(g\right)\)
b) \(n_{Fe_2O_3\left(dư\right)}=0,3-\dfrac{1}{15}=\dfrac{7}{30}\left(mol\right)\)
PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\)
Theo PT: \(n_{HCl}=2n_{Fe}+6n_{Fe_2O_3}=\dfrac{5}{3}\left(mol\right)\)
`=>` \(m_{ddHCl}=\dfrac{\dfrac{5}{3}.36,5}{3,65\%}=\dfrac{5000}{3}\left(g\right)\)
c) Theo PT: \(n_{H_2}=n_{Fe}=\dfrac{2}{15}\left(mol\right)\)
`=>` \(m_{ddspư}=\dfrac{5000}{3}+44,8-\dfrac{2}{15}.2=1711,2\left(g\right)\)
Theo PT: \(\left\{{}\begin{matrix}n_{FeCl_2}=n_{Fe}=\dfrac{2}{15}\left(mol\right)\\n_{FeCl_3}=2n_{Fe_2O_3}=\dfrac{7}{15}\left(mol\right)\end{matrix}\right.\)
`=>` \(\left\{{}\begin{matrix}C\%_{FeCl_2}=\dfrac{\dfrac{2}{15}.127}{1711,2}.100\%=1\%\\C\%_{FeCl_3}=\dfrac{\dfrac{7}{15}.162,5}{1711,2}.100\%=4,43\%\end{matrix}\right.\)
cảm ơn bạn