Cho 2,81 gam hỗn hợp Fe2O3, ZnO, MgO tác dụng vừa đủ với dung dịch có 0.05 mol H2SO4. Khối lượng muối sunfat tạo ra trong dung dịch là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Áp dụng phương pháp tăng giảm khối lượng.
Cứ 1 mol H2SO4 phản ứng, để thay thế O (trong oxit) bằng S O 4 2 - trong các kim loại, khối lượng tăng 96 - 16 = 80 g. Theo đề số mol H2SO4 phản ứng là 0,03 thì khối lượng tăng 0,24 g.
Vậy khối lượng muối khan thu được là: 2,81 + 2,4 = 5,21
Đáp án C

PTHH: Oxit + H2SO4 \(\rightarrow\) muối + H2O
Bảo toàn nguyên tố H => nH2O = nH2SO4 = 0,5.0,1 = 0,05 mol
Áp dụng định luật bảo toàn khối lượng ta có:
=> moxit+ mH2SO4 = mmuối+ mH2O
=> mmuối= 2,81 + 0,05.98 - 0.05.18 = 6,81g

\(n_{H_2SO_4}=0.1\cdot0.25=0.025\left(mol\right)\)
\(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
\(ZnO+H_2SO_4\rightarrow ZnSO_4+H_2O\)
\(MgO+H_2SO_4\rightarrow MgSO_4+H_2O\)
\(TừPTHH:\)
\(n_{H_2SO_4}=n_{H_2O}=0.025\left(mol\right)\)
\(BTKL:\)
\(m_{Muối}=1.405+0.025\cdot98-0.025\cdot18=3.405\left(g\right)\)

Chọn A
Cần nhớ phản ứng cho oxit bazơ tác dụng với H 2 S O 4 thì:

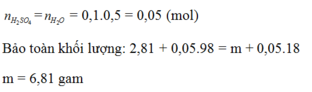



$Fe_2O_3 + 3H_2SO_4 \to Fe_2(SO_4)_3 + 3H_2O$
$ZnO + H_2SO_4 \to ZnSO_4 + H_2O$
$MgO + H_2SO_4 \to MgSO_4 + H_2O$
Theo PTHH : $n_{H_2O} = n_{H_2SO_4} = 0,05(mol)$
Bảo toàn khối lượng :
$m_{muối} = m_{hh} + m_{H_2SO_4} - m_{H_2O} = 2,81 + 0,05.98 - 0,05.18 = 6,81(gam)$
Fe2O3+ H2SO4--->FeSO4+H2O
ZnO +H2SO4---> ZnSO4+ H2O
MgO+ H2SO4---->MgSO4+H2O
Do nH2SO4=0,05
=>mH2SO4= 0,05.98=4,9 (g)
Theo pt :nH2O=nH2SO4 =0,05 MOL
mH2O=0,05.18=0,9 (g)
ADDLBTKL ta có :2,81+4,9=m muối+0,9
=> m muối=6,81(g)