Bài 1 : Ta dùng 8 tấn quặng pirit Fe ( chứa 60% FeS2 ) để sản xuất H2SO4. Tính khối lượng dung dịch H2SO4 60% thu được biết hiệu suất của quá trình sản xuất đạt 75%.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(m_{H_2SO_4}=\dfrac{1000000.98\%}{100\%}=980000(g)\\ \Rightarrow n_{H_2SO_4}=\dfrac{980000}{98}=10000(mol)\\ \Rightarrow n_{FeS_2}=\dfrac{1}{2}n_{H_2SO_4}.80\%=4000(mol)\\ \Rightarrow m_{FeS_2}=4000.120=480000(g)\)

Đáp án C.
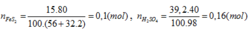
FeS2→ 2H2SO4
0,08 ← 0,16 (mol)
H% = 0,08.100/0,1= 80%

Đáp án C
FeS2 → Fe → thép không gỉ.
Khối lượng quặng thực tế: 12 . 0 , 74 . 120 56 . 0 , 6 . 0 , 8 = 3 , 7 ( tấn )

\(TQ:FeS_2->2SO_2->2SO_3->2H_2SO_4\\ m_{FeS_2}=\dfrac{1\cdot120}{98\cdot2\cdot0,7}=0,8746\left(\text{tấn }\right)\)

Câu 1:
Ta có: 1 tấn = 1000 kg
⇒ mFe = 1000.95% = 950 (kg)
\(\Rightarrow n_{Fe}=\dfrac{950}{56}\left(kmol\right)\)
BTNT Fe, có: \(n_{Fe_2O_3\left(LT\right)}=\dfrac{1}{2}n_{Fe}=\dfrac{475}{56}\left(kmol\right)\)
Mà: H = 80% \(\Rightarrow n_{Fe_2O_3\left(TT\right)}=\dfrac{475}{56}:80\%=\dfrac{2375}{224}\left(kmol\right)\)
\(\Rightarrow m_{Fe_2O_3\left(TT\right)}=\dfrac{2375}{224}.160=\dfrac{11875}{7}\left(kg\right)\)
⇒ m quặng \(=\dfrac{m_{Fe_2O_3}}{60\%}\approx2827,38\left(kg\right)\)
Câu 2:
Ta có: 65nZn + 27nAl = 3,79 (1)
PT: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
Theo PT: \(n_{H_2}=n_{Zn}+\dfrac{3}{2}n_{Al}=\dfrac{1,792}{22,4}=0,08\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Zn}=0,05\left(mol\right)\\n_{Al}=0,02\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Zn}=0,05.65=3,25\left(g\right)\\m_{Al}=0,02.27=0,54\left(g\right)\end{matrix}\right.\)
Ta có: \(m_{FeS_2}=60\%.8=4,8\left(tấn\right)\)
\(FeS_2\rightarrow2S\)
120(g)->64(g)
4,8(tấn)->2,56(tấn)
\(S\rightarrow H_2SO_4\)
32(g)->98(g)
2,56(tấn)->7,84(tấn)
`=>` \(m_{ddH_2SO_4\left(60\%.TT\right)}=\dfrac{7,84.75\%}{60\%}=9,8\left(tấn\right)\)
Ta có: mFeS2 = 8.60% = 4,8 (tấn) = 4800 (kg)
\(\Rightarrow n_{FeS_2}=\dfrac{4800}{120}=40\left(kmol\right)\)
BTNT S, có: \(n_{H_2SO_4\left(LT\right)}=2n_{FeS_2}=80\left(kmol\right)\)
Mà: H% = 75% \(\Rightarrow n_{H_2SO_4\left(TT\right)}=80.75\%=60\left(kmol\right)\)
\(\Rightarrow m_{H_2SO_4\left(TT\right)}=60.98=5880\left(kg\right)\)
\(\Rightarrow m_{ddH_2SO_4\left(60\%\right)}=\dfrac{5880}{60\%}=9800\left(kg\right)\)