Cho 86,3 gam hỗn hợp X gồm Na, K, Ba và Al2O3 ( trong đó oxi chiếm 19,47% về khối lượng) tan hết vào nước, thu được dung dịch Y và 13,44 lít khí H2 ( đktc). Cho V lít dd HCl 2M vào dd, sau khi các phản ứng xảy ra hoàn toàn thu được 46,8 gam kết tủa. Tính thể tích dd HCl đã dùng.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Giải thích:
mO(X)=86,3.19,47/100=16,8 gam=>nO(X)=1,05 mol=>nAl2O3=nO(X)/3=0,35 mol.
nOH-=2nH2=1,2 mol.
nHCl=3,2.0,75=2,4 mol.
Al2O3+2OH-→2AlO2- +H2O
0,35 0,7 0,7(mol)
Y gồm: 0,5 mol OH- dư, 0,7 mol AlO2-
H+ + OH-→H2O
0,5←0,5 (mol)
H+ + AlO2- + H2O→Al(OH)3↓
0,7←0,7→ 0,7 (mol)
Al(OH)3↓+3H+→Al3++3H2O
0,4←2,4-0,5-0,7=1,2 (mol)
nAl(OH)3=0,7-0,4=0,3 mol =>m↓=0,3.78=23,4 g.
Đáp án A

Đáp án D
Theo đề bài ta có
![]()
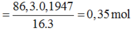
Khi hòa tan hỗn hợp X bằng nước.Xét dung dịch Y ta có :
![]()
![]()
![]()
- Khi cho dung dịch Y tác dụng với 2,4 mol HCl, vì:
![]()

![]()

Đáp án A
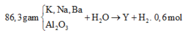
Từ số mol H2 ta tính được số mol O H - giải thích
![]()
![]()
![]() , mà
A
l
2
O
3
→
3
O
, mà
A
l
2
O
3
→
3
O
→ n A l 2 O 3 = 0 , 35 m o l
⇒ n O H - = 2 n H 2 = 1 , 2 m o l
Ta có phương trình:
![]()
=> dung dịch Y gồm

⇒ kết tủa A l ( O H ) 3
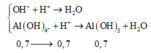
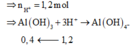
=> Số mol kết tủa còn lại là:
![]()
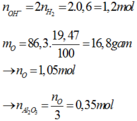
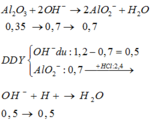
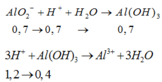
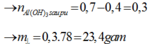



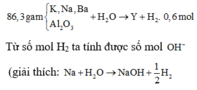

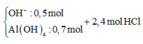

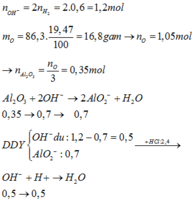
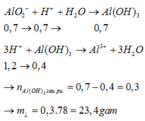


$n_O = \dfrac{86,3.19,47\%}{16} = 1,05(mol)$
Coi hỗn hợp gồm $Na(a\ mol) , Al(b\ mol)$ và O(1,05 mol)
Ta có :
$23a + 27b + 1,05.16 = 86,3(1)$
Bảo toàn electron : $n_{Na} + 3n_{Al} = 2n_O + 2n_{H_2}$
$\Rightarrow a + 3b = 1,05.2 + 0,6.2(2)$
Từ (1)(2) suy ra $a = \dfrac{199}{70} ; b = \dfrac{16}{105}$
Suy ra Y gồm :
$AlO_2^- : \dfrac{16}{105}(mol)$
$Na^+ : \dfrac{199}{70}(mol)$
$OH^- : \dfrac{199}{70} - \dfrac{16}{105} = \dfrac{113}{42}(mol)$
$n_{Al(OH)_3} = \dfrac{46,8}{78} = 0,6(mol)$
Suy ra :
$n_{HCl} = n_{H^+} = n_{OH^-} + 4n_{AlO_2^-} - 3n_{Al(OH)_3} = 1,5(mol)$
$V_{dd\ HCl} = \dfrac{1,5}{2} = 0,75(lít)$