Điện phân dung dịch chứa m gam hỗn hợp CuSO4 và NaCl (điện cực trơ, màng ngăn xốp, hiệu suất điện phân 100%, bỏ qua sự hòa tan của khí trong nước và sự bay hơi của nước), cho đến khi nước bắt đầu bị điện phân ở cả hai điện cực thì dừng lại, thu được 0,896 lít (đktc) khí ở anot. Dung dịch sau khi điện phân có thể hòa tan tối đa 3,2 gam CuO. Giá trị của m là: A. 11,94. B. 9,60. C. 5,97. D. 6,40.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
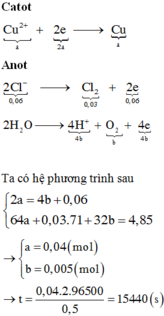
- Nếu cả 2 bị điện phân hết thì mgiảm = 0,05*64 + 0,03*71 > 4.85. vậy:
+ TH1: Cu2+ chưa hết
Catot......................... 0,05 mol CuSO4 + 0,06 mol NaCl...................................... anot
Na+ SO42-
Cu2+ + 2e = Cu 2Cl- = Cl2 + 2e
x → 2x → x 0,06......0,03......0,06
H2O = O2 + 4H + 4e
y......4y......4y
- mgiảm = 64x + 71*0,03 + 32y = 4,85
- BT e: 0,06 + 4y = 2x
- Giải x = 0,04 và y = 0,005
- t = (ne*F):I = 0,08*96500/0,5 = 15440.

Đáp án C
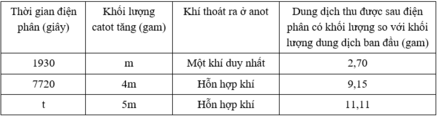
Do tại 3 thời điểm khối lượng catot đều tăng nên Cu2+ điệp phân chưa hết ở t1 và t2
*Tại t1 = 1930 giây: ne1 = It1/F = 0,02I
=> nCl2 = 0,01I
n e1 = 2nCu2+ bị đp => 0,02I = 2m/64 (1)
m dung dịch giảm = mCu + mCl2 => 2,7 = m + 71.0,01I (2)
Giải (1) và (2) => m = 1,28; I = 2
*Tại t2 = 7720 => ne2 = 0,16 mol
Anot:
Cl- -1e → 0,5Cl2
x 0,5x
H2O -2e → 0,5O2 + 2H+
y 0,25y
x+y = 0,16
0,5x.71+0,25y.32+4.1,28 = 9,15
Giải ra ta được x = 0,1; y = 0,06
*Tại t3 = t: Giả sử nước bị điện phân ở cả 2 điện cực
nH2 = a mol, nO2 = b mol
m dung dịch giảm = mCu + mH2 + mCl2 +mO2 => 11,11 = 5.1,28 + 2a + 0,05.71 + 32b (3)
n e anot = ne catot => 2nCu + 2nH2 = 2nCl2 + 4nO2 => 2.0,1 + 2a = 0,05.2 + 4b (4)
Giải (3) và (4) thu được: a = 0,02; b = 0,035
n e3 = 2.0,1 + 2.0,02 = 0,24 mol => t = 0,24.96500/2 = 11580 giây

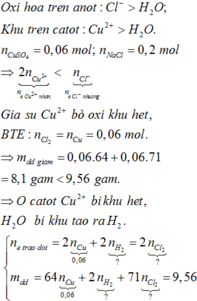
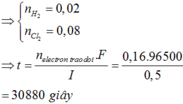
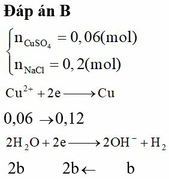
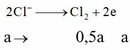



A
Dung dịch sau điện phân có \(H^+\) nên hòa tan được \(\dfrac{3,2}{80}\) \(=0,04\) mol \(CuO\)
\(\rightarrow n_{H+}=2n_{CuO}\)\(=0,08\left(mol\right)\)
\(n\)khí anot \(=0,04\left(mol\right)\)
\(\left(-\right)\)Catot:
\(Cu^2+2e\rightarrow Cu\)
\(\left(+\right)\):Anot:
\(2Cl^-\rightarrow Cl_2+2e\)
\(2H_2O\rightarrow4H^++O2+4e\)
\(n_{O_2}=\dfrac{n_{H^+}}{4}=0,02\left(mol\right)\)
\(\rightarrow n_{Cl_2}=0,04-0,02=0,02\left(mol\right)\)
\(\rightarrow n_{NaCl}=0,02.2=0,04\left(mol\right)\)
BTe:\(2n_{Cu}=2n_{Cl_2}+4n_{O_2}\)
\(\rightarrow n_{CuSO_4}=n_{Cu}=0,06\left(mol\right)\)
Vậy \(m=0,06.160+0,04.58,5=11,94g\)
thanks