iriđi có 2 đồng vị bền:191/77 IR và 193/77. Nguyên tử khối trung bình của ir là 192,22
a hãy tính phần trăm số nguyên tử và phần trăm gần đúng của mỗi đồng vị (39%-61%)
b giả sử có 15 nguyên tử 191/77 IR thì có bao nhiêu nguyên tử 193/77 iR
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

ta có
191x1+193x2=19222(1)
x1+x2=100(2)
Từ 1 và 2 ta có hpt
191x1+193x2=19222 và x1+x2=100
ta giải hệ đc
x1=39 ; x2=61

Gọi \(\%^{35}Cl\) là \(x\); \(\%^{37}Cl\) là \(y\)
Ta có:\(x+y=100\left(1\right)\)
Nguyên tử khối trung bình:
\(\overline{M_{Cl}}=\dfrac{35x+37y}{100}=35,5\Rightarrow35x+37y=3550\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=75\%\\y=25\%\end{matrix}\right.\)

Đáp án D
Gọi thành phần phần trăm của 191Ir và 193Ir lần lượt x, y
Ta có hệ

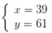
Phần trăm số nguyên tử của 193Ir là 61%

a) Đặt %24Mg là x
-->%25Mg là (100 - x - 11)
\(\overline{M}=\dfrac{x.24+\left(100-x-11\right).25+11.26}{100}=24,32\)
\(\Rightarrow x=\%^{24}Mg=79\%\)
b) ta có : \(n_{Mg}=n_{MgCl2}=1\left(mol\right)\Rightarrow n_{26_{Mg}}=1.11\%=0,11\left(mol\right)\)
Số nguyên tử : \(0,11.6,022.10^{-3}=6,6022.10^{-4}\)(nguyên tử)

- Gọi tỉ lệ đồng vị 35Cl trong tự nhiên là x%
=> Tỉ lệ đồng vị 37Cl trong tự nhiên là (100-x)%
- Nguyên tử khối trung bình của Cl là 35,45
=> \(35,45 = \frac{{35.x + 37.(100 - x)}}{{100}}\)
=> x = 77,5
Vậy đồng vị 35Cl chiếm 77,5% trong tự nhiên, đồng vị 37Cl chiếm 22,5% trong tự nhiên.
a) Gọi phần trăm của 2 đồng vị \(^{191}_{77}Ir\) và \(^{193}_{77}Ir\) lần lượt là x% và y%
`=>` \(\left\{{}\begin{matrix}x+y=100\\191.0,01x+193.0,01y=192,22\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=39\%\\y=61\%\end{matrix}\right.\)
b) Số nguyên tử \(^{193}_{77}Ir\) là: \(15.\dfrac{61}{39}=\dfrac{305}{13}\) (nguyên tử)