Hỗn hợp A1 gồm Al2O3 và Fe2O3. Dẫn khí CO qua 21,1 gam A1 và nung nóng thu được hỗn hợp A2 gồm 5 chất rắn và hỗn hợp khí A3. Dẫn A3 qua dung dịch Ca(OH)2 dư thấy có 5 gam kết tủa. A2 tác dụng vừa đủ với 1 lít dung dịch H2SO4 0,5M thu được dung dịch A4 và có 2,24 lít khí thoát ra ( đktc ). Tính % khối lượng mỗi chất trong hỗn hợp A1.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án : B
nCO2 = nO pứ =nCaCO3 = 0,15 mol
nH2SO4 = 0,35 mol ; nH2 = 0,05 mol
Bảo toàn H : nH2SO4 = nH2 + nH2O => nH2O = 0,3 mol = nO (oxit)
=> nO bđ =0,3 + 0,15 = 0,45 mol
=> 3nAl2O3 + 3nFe2O3 = 0,45 mol
Và 102nAl2O3 + 160nFe2O3 = 21,1g
=> nAl2O3 = 0,05 mol ; nFe2O3 = 0,1 mol
=> %mAl2O3 = 24,17%

A 1 là CO, C O 2 ; A 2 là C O 2 ; A 3 là Cu, CuO dư; A 4 là C a C O 3 ; A 5 là C a H C O 3 2

⇒ Chọn A.

Trong trường hợp này, X đã “bão hòa”, không thể cho e được nữa, nhưng nó đã được CO lấy đi một lượng O để phá vỡ trạng thái này. CO + [O] →CO2
Và thế là X trở thành Y, lại có thể cho e với N+5 tạo thành NO, NO2.
Theo lý thuyết, nếu HNO3 lại đưa Y lên trạng thái bão hòa thì số mol e mà N+5 nhận được là 0,24 x 2 = 0,48 mol
Nhưng trên thực tế, con số này là 0,11 x 3 + 0,07 x 1= 0,40 mol
Sở dĩ điều này xảy ra là do có một lượng Fe chỉ tồn tại ở số oxi hóa +2
→ nFe2+ = 0,48 – 0,40 =0,08 → mFe(NO3)2 = 14,4 gam
Chọn đáp án C

Đáp án A.
→ n X = 0 , 5 ; n C O 2 = 0 , 15 ; n C O = 0 , 1 → n N 2 = 0 , 25
→
n
X
=
0
,
25
→
n
C
a
C
O
3
=
n
C
O
+
n
C
O
2
=
0
,
125
→
m
=
12
,
5

Đáp án A.
![]()
![]()
→ n X = 0 , 25 → n C a C O 3 = n C O + n C O 2 = 0 , 125 → m = 12 , 5
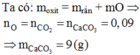



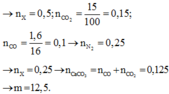
PTHH:
\(3Fe_2O_3+CO\xrightarrow[]{t^o}2Fe_3O_4+CO_2\) (1)
\(Fe_3O_4+CO\xrightarrow[]{t^o}3FeO+CO_2\) (2)
\(FeO+CO\xrightarrow[]{t^o}Fe+CO_2\) (3)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3\downarrow+H_2O\) (4)
\(Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O\) (5)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\) (6)
\(FeO+H_2SO_4\rightarrow FeSO_4+H_2O\) (7)
\(Fe_3O_4+4H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+FeSO_4+4H_2O\) (8)
\(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\) (9)
Ta có: \(\left\{{}\begin{matrix}n_{CaCO_3}=\dfrac{5}{100}=0,05\left(mol\right)\\n_{H_2SO_4}=0,5.1=0,5\left(mol\right)\\n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\end{matrix}\right.\)
BTNT C: \(n_{CO_2}=n_{CaCO_3}=0,05\left(mol\right)\)
Theo PT (1), (2), (3): \(n_{O\left(pư\right)}=n_{CO_2}=0,05\left(mol\right)\)
Theo PT (5), (6), (7), (8), (9): \(n_{H_2SO_4}=n_{O\left(còn,lại\right)}+n_{H_2}\)
=> \(n_{O\left(còn.lại\right)}=0,5-0,1=0,4\left(mol\right)\)
=> \(n_{O\left(bđ\right)}=0,4+0,05=0,45\left(mol\right)\)
Gọi \(\left\{{}\begin{matrix}n_{Al_2O_3}=x\left(mol\right)\\n_{Fe_2O_3}=y\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}102x+160y=21,1\\3x+3y=0,45\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,05\\y=0,1\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}\%m_{Al_2O_3}=\dfrac{0,05.102}{21,1}.100\%=24,17\%\\\%m_{Fe_2O_3}=100\%-24,17\%=75,83\%\%\end{matrix}\right.\)
ah ơi cho e hỏi 3 hàng này là sao vậy ạ, ah giải thích cho e với