Cho hỗn hợp bột gồm 5,4 gam Al và 11,2 gam Fe vào 800ml dung dịch AgNO3 1M. Sau khi các phản ứng xảy ra hoàn toàn thu được m gam chất rắn. Giá trị của m là
K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Những câu hỏi liên quan

6 tháng 12 2018
Đáp án : D
nAl = 0,2 mol ; nFe = 0,2 mol ; nAgNO3 = 0,8 mol
Các phản ứng có thể xảy ra :
Al + 3Ag+ -> Al3+ + 3Ag
Fe + 2Ag+ -> Fe2+ + 2Ag
Fe2+ + Ag+ -> Fe3+ + Ag
=> nAg = 0,8 mol
=> nFe dư = 0,2 – 0,1 = 0,1 mol
=> mrắn = 0,8.108 + 0,1.56 = 92g
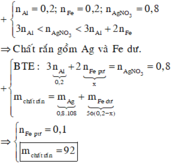

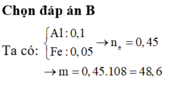
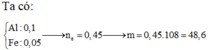


$n_{Al} = \dfrac{5,4}{27} = 0,2(mol)$
$n_{Fe} = \dfrac{11,2}{56} = 0,2(mol)$
$n_{AgNO_3} = 0,8(mol)
\(Al+3AgNO_3\text{→}Al\left(NO_3\right)_3+3Ag\)
0,2 0,6 0,6 (mol)
\(Fe+2AgNO_3\text{→}Fe\left(NO_3\right)_2+2Ag\)
0,1 0,2 0,2 (mol)
Sau phản ứng, $n_{Fe\ dư} = 0,2 - 0,1 = 0,1(mol) ; n_{Ag} = 0,6 + 0,2 = 0,8(mol)$
$m = 0,1.56 + 0,8.108 = 92(gam)$