HNO3 0,1 m vào 300 ml dung dịch baoh2 0,1 m Thu được dung dịch x tính pH của dung dịch x
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Ta có: \(n_{KOH}=0,05.0,1=0,005\left(mol\right)\)
\(n_{HNO_3}=0,052.0,1=0,0052\left(mol\right)\)
PT: \(KOH+HNO_3\rightarrow KNO_3+H_2O\)
Xét tỉ lệ: \(\dfrac{0,005}{1}< \dfrac{0,0052}{1}\), ta được HNO3 dư.
Theo PT: \(n_{HNO_3\left(pư\right)}=n_{KOH}=0,005\left(mol\right)\)
\(\Rightarrow n_{H^+}=n_{HNO_3\left(dư\right)}=0,0002\left(mol\right)\)
\(\Rightarrow\left[H^+\right]=\dfrac{0,0002}{0,05+0,052}=\dfrac{1}{510}\left(M\right)\)
⇒ pH = -log[H+] ≃ 2,71

\(1.n_{cation}=0,1.0,6+0,05.0,4=0,08\left(mol\right)\\ C_{M\left(cation\right)}=\dfrac{0,08}{0,6+0,4}=0,08\left(M\right)\\ 2.n_{cation}=0,2.0,2+2.0,3.0,1=0,1mol\\ C_{M\left(cation\right)}=\dfrac{0,1}{0,2+0,3}=0,2\left(M\right)\)
Cation của H2SO4 là H+.
Đề yêu cầu tính tổng nồng độ, không phải tổng số mol.

Chọn A
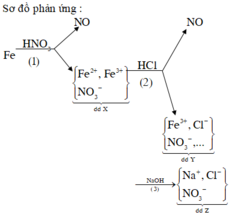
nOH- = 0,06x2 = 0,12 > nNH3 = 0,08 Þ OH- dư Þ Trong X có chứa nNH4+ = 0,08
BTĐT => n S O 4 2 - = (0,12 + 0,08 - 0,l)/2 = 0,05 < nBa2+ = 0,06 Þ Có 0,05 mol BaSO4 kết tủa
Þ Trong Z có nBa2+ = 0,06 - 0,05 = 0,01; nK+ = 0,12; nCl- = 0,1; nOH- = 0,12 - 0,08 = 0,04
Vậy m = 0,01x137 + 0,12x39 + 0,1x35,5 + 0,04x17 = 10,28.

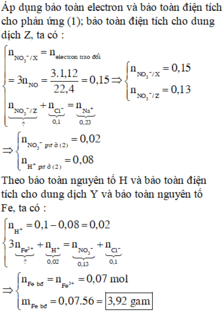
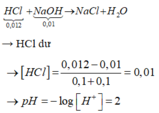
Số mol H+ ban đầu là 0,1.V1 (với V1 là thể tích HNO3 ban đầu).
Số mol OH- ban đầu là 0,1.0,3 = 0,03 (mol).
Trong dung dịch X:
Nếu ion H+ dư thì pH<7.
Nếu ion OH- dư thì pH>7.
Nếu ion H+ bằng ion OH- thì pH=7.