Cho 1,35 gam hỗn hợp A gồm Cu, Mg, Al tác dụng với H2SO4 đặc nóng dư được 0,784 lít khí SO2 (đktc,spk duy nhất). Tổng khối lượng muối sunfat sinh ra là?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


nSO2 = \(\dfrac{2,8}{22,4}\)=0,125 mol
S+6 + 2e → S+4
0,25<-----0,125
=> Số mol e do 3,35 gam hỗn hợp kim loại nhường là 0,25 mol.
Xét phản ứng với Clo
Kim loại + Cl2 → Muối clorua
Có 3,35 gam kim loại phản ứng nên số mol e kim loại nhường cũng là 0,25 mol
Cl20 + 2e → 2Cl-1
0,25 --> 0,25
=> nCl-1 trong muối clorua = 0,25 mol
<=> mCl-1 = 0,25.35,5 = 8,875 gam.
mMuối = mKim loại + mCl-1 = 3,35 + 8,875 = 12,225 gam.

Đáp án C
Gọi n N O = a n N O 2 = b
Có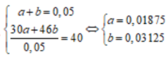
Vậy
m m u ố i = m k i m l o ạ i + m N O 3 -
=1 1,35+62.0,0875 = 6,775 (gam)

Theo gt ta có: $n_{NO}=0,01(mol);n_{NO_2}=0,04(mol)$
Bảo toàn e ta có: $n_{e}=n_{NO_3^-/trongmuoi}=0,07(mol)$
$\Rightarrow m_{muoi}=1,35+62.0,07=5,69(g)$

Gọi \(n_{NO} = a ; n_{NO_2} = b\)
Ta có :
\(a + b = \dfrac{896}{1000.22,4} = 0,04\\ 30a + 46b = 0,04.42\)
Suy ra a = 0,01 ; b = 0,03
Giả sử không có muối amoni tạo thành.
\(n_{NO_3^-} = n_{e\ trao\ đổi} = 3n_{NO} + n_{NO_2} = 0,06(mol)\)
\(m_{muối} = m_{kim\ loại} + m_{NO_3^-} = 1,35 + 0,06.62 = 5,07(gam)\)

`2Fe + 6H_2 SO_[4(đ,n)] -> Fe_2(SO_4)_3 + 3SO_2 \uparrow + 6H_2 O`
`0,05` `0,15` `0,025` `(mol)`
`Cu + 2H_2 SO_[4(đ,n)] -> CuSO_4 + SO_2 \uparrow + 2H_2 O`
`0,225` `0,45` `0,225` `(mol)`
`n_[SO_2]=[6,72]/[22,4]=0,3(mol)`
Gọi `n_[Fe]=x` ; `n_[Cu]=y`
`=>` $\begin{cases} \dfrac{3}{2}x+y=0,3\\56x+64y=17,2 \end{cases}$
`<=>` $\begin{cases}x=0,05\\y=0,225 \end{cases}$
`@m_[Fe_2(SO_4)_3]=0,025.400=10(g)`
`@m_[CuSO_4]=0,225.160=36(g)`
`@m_[dd H_2 SO_4]=[(0,15+0,45).98]/80 .100=73,5(g)`
Sửa đề: 80% ---> 98% (80% chưa đặc nên không giải phóng SO2 được)
Gọi \(\left\{{}\begin{matrix}n_{Fe}=a\left(mol\right)\\n_{Cu}=b\left(mol\right)\end{matrix}\right.\)
\(\rightarrow56a+64b=17,2\left(1\right)\)
PTHH:
\(2Fe+6H_2SO_{4\left(đặc,nóng\right)}\rightarrow Fe_2\left(SO_4\right)_3+3SO_2\uparrow+6H_2O\)
a------>3a------------------->0,5a--------------->1,5a
\(Cu+2H_2SO_{4\left(đặc,nóng\right)}\rightarrow CuSO_4+SO_2\uparrow+2H_2O\)
b----->2b------------------->b------------->b
\(\rightarrow1,5a+b=\dfrac{6,72}{22,4}=0,3\left(2\right)\)
Từ \(\left(1\right)\left(2\right)\rightarrow\left\{{}\begin{matrix}a=0,05\left(mol\right)\\b=0,225\left(mol\right)\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}m_{Fe_2\left(SO_4\right)_3}=0,5.0,05.400=10\left(g\right)\\m_{CuSO_4}=0,225.160=36\left(g\right)\\m_{ddH_2SO_4}=\dfrac{\left(0,05.3+0,225.2\right).98}{98\%}=60\left(g\right)\end{matrix}\right.\)

Đáp án : A
P1 : ne trao đổi = nNO2 = 0,47 mol
P2 : ne trao đổi = nCl2 .2 => nCl2 pứ = 0,235 mol
=> mKL = mmuối – mCl2 pứ = 11,19g
=> m = 2.11,19 = 22,38g

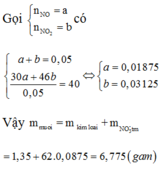

n SO2=\(\dfrac{0,784}{22,4}=0,035mol\)
=>n H2SO4 =2nSO2=0,035.2=0,07 mol
Bảo toàn nguyên tố S: n gốc axit =n H2SO4 -nSO2=0,035
=>m muối=1,35+0,035.96=4,71g