Cho 61,2g hỗn hợp X gồm Cu và Fe3O4 tác dụng với dung dịch HNO3 loãng, đun nóng và khuấy đều. Saukhi các phản ứng xảy ra hoàn toàn thu được 3,36 l NO (sản phẩm khử duy nhất, đktc), dung dịch Y và còn lại 2,4g kim loại. Cô cạn dung dịch Y thu được m g muối khan. Giá trị của m là:
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A:
nNO = 0,15 (mol), kim loại còn lại sau phản ứng là Cu.
nCu dư =0,0375(mol)
nX phản ứng= 61,2 - 2,4 = 58,8 (g)
Đặt x và y lần lượt là số mol Cu và Fe3O4.
Quy Fe3O4 thành hỗn hợp FeO và Fe2O3 có tỉ lệ mol 1:1
Theo khối lượng X => 64x+232y = 58,8
Bảo toàn electron ta có: ne cho= nenhận
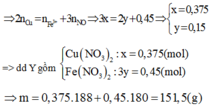

Quy đổi X thành các đơn chất: Cu (x mol); Fe (l,5y mol); O2 (y mol) => 64x + 116y = 61,2 - 2,4 = 58,8
Bảo toàn electron ta có: ne cho = ne nhận
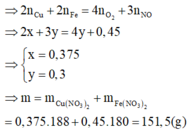
Đáp án B

Chọn C.
Ta có: nNO = 0,15 mol.
Gọi a là số mol Cu trong X đã phản ứng; b là số mol Fe3O4 trong X, ta có:
64a + 232b = 61,2 - 2,4
Các nguyên tố Cu, Fe, O trong hỗn hợp X khi phản ứng với HNO3 chuyển thành muối Cu2+, Fe2+ (vì dư kim loại), H2O do đó theo định luật bảo toàn electron, ta có:
2a + 2.3b - 2.4b = 3.0,15 → a = 0,375; b = 0,15
Muối khan gồm: Cu(NO3)2 (a = 0,375 mol) và Fe(NO3)2 (3b = 0,45 mol)
→ mmuối = 188.0,375 + 180.0,45 = 151,5 gam

nNO = 0,15 (mol)
Gọi a là số mol Cu trong X đã phản ứng. Gọi b là số mol Fe3O4 trong X
Ta có: 64a + 232b = 61,2 – 2,4
Các nguyên tố Cu, Fe, O trong hỗn hợp X khi phản ứng với HNO3 chuyển thành muối Cu2+, Fe2+ (vì dư kim loại), H2O do đó theo bảo toàn e: 2a + 2.3b – 2.4b = 3.0,15
Từ đó: a = 0,375; b = 0,15
Muối khan gồm có: Cu(NO3)2 (a = 0,375 mol) và Fe(NO3)2 (3b = 0,45 mol)
mmuối = 188.0,375 + 180.0,45 = 151,5 (gam)
Đáp án B

Định hướng tư duy giải:
Vì có kim loại dư (Cu) nên muối chỉ là muối Fe2+ và Cu2+.Ta đó đầu bằng các BTE cho cả quá trình. Khi đó
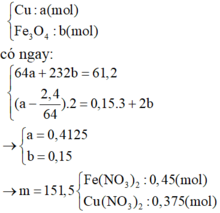


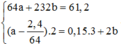
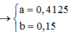
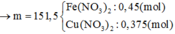
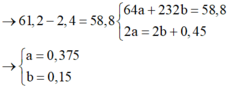
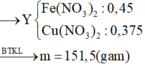
Sau phản ứng Cu dư
$n_{NO} = \dfrac{3,36}{22,4} = 0,15(mol)$
Gọi $n_{Cu\ pư} = a(mol) ; n_{Fe_3O_4} = b(mol) \Rightarrow 64a+232b + 2,4 = 61,2(1)$
$Cu^0 \to Cu^{+2} + 2e$
$3Fe^{ \dfrac{+8}{3}} + 2e \to 3Fe^{+2}$
$N^{+5} + 3e \to N^{+2}$
Bảo toàn electron :$2n_{Cu} = 2n_{Fe_3O_4} + 3n_{NO}$
$\Rightarrow 2a = 2b + 0,15.3(2)$
Từ (1)(2) suy ra : a = 0,375 ; b = 0,15
$n_{Cu(NO_3)_2} = a = 0,375(mol)$
$n_{Fe(NO_3)_2} = 3n_{Fe_3O_4} = 0,45(mol)$
$\Rightarrow m = 0,375.188 + 0,45.180 = 151,5(gam)$
2,4 gam kim loại là Cu dư => dd muối thu được gồm 2 muối Cu(NO3)2, Fe(NO3)2
Gọi \(\left\{{}\begin{matrix}n_{Cu\left(pư\right)}=x\left(mol\right)\\n_{Fe_3O_4}=y\left(mol\right)\end{matrix}\right.\)
=> 64x + 232y = 61,2 - 2,4 = 58,8 (*)
\(n_{NO}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Quá trình oxi hoá - khử:
\(Cu^0\rightarrow Cu^{+2}+2e\)
\(3Fe^{+\dfrac{8}{3}}+2e\rightarrow3Fe^{+2}\)
\(N^{+5}+3e\rightarrow N^{+2}\)
Bảo toàn electron: \(2n_{Cu}=2n_{Fe_3O_4}+3n_{NO}\)
=> 2x - 2y = 0,45 (**)
Từ (*), (**) => x = 0,375 (mol); y = 0,15 (mol)
Theo BTNT Cu, Fe: \(\left\{{}\begin{matrix}n_{Cu\left(NO_3\right)_2}=n_{Cu\left(pư\right)}=0,375\left(mol\right)\\n_{Fe\left(NO_3\right)_2}=3n_{Fe_3O_4}=0,45\left(mol\right)\end{matrix}\right.\)
=> m = 0,375.188 + 0,45.180 = 151,5 (g)