Hòa tan hoàn toàn 2,44g X gồm FexOy và Cu bằng dd H2SO4 đặc nóng dư tạo thành 0,504l SO2 và dd chứa 6,6g hh muối sunfat.Xác định %mCu trong X và công thức FexOy
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án C
Coi hỗn hợp X gồm các nguyên tố Fe (x mol) , O (y mol) và Cu (z mol).
=> Hai muối sunfat là Fe2(SO4)3 (x/2 mol) và CuSO4 (z mol)


Giả sử số mol FexOy,Cu lần lượt là a,b mol
PTPU: 2FexOy + (6x-2y)H2SO4(đn) -> xFe2(SO4)3 + (3x-2y)SO2 + (6x-2y) H2O
a ax/2 a(3x-2y)/2 (mol)
Cu + 2H2SO4(đn) -> CuSO4 + SO2 +2H2O
b b b (mol)
nSO2=0,504/22,4=0,0225 mol
Theo bài ra và PTPU ta có hệ
- a(56x+16y) + 64b =2,44
- ax/2 .200 + 160b =6,6
- a(3x-2y) + b= 0,0225
=> ax=0,025 , ay= 0,025, b=0,01
=>x=1, y=1 => FexOy là FeO
%mCu=64.0,01 / 2,44 .100% = 26,23%

Bạn xem hỗn hợp ban đầu được tạo thành từ: Fe, Cu và O2
Fe -------> Fe3+ + 3e
x.........................3x
Cu -------> Cu2+ + 2e
y..........................2y
O2 + 4e -----> 2O2-
z.........4z
S+6 + 2e -------> S+4
...........0,045..........0,0225
Gọi x, y, z là số mol Fe, Cu, O2. Ta có hpt:
56x + 64y + 32z = 2,44
3x + 2y = 4z + 0,045
0,5*400x + 160y = 6,6
=> x = 0,025, y = 0,01, z = 0,0125
=> %mCu = 0,01*64/2,44*100% = 26,23%

Có nSO2 = 0,225 mol
Coi hỗn hợp gồm x mol Fe; y mol O ; z mol Cu.
Cho X vào H2SO4 thì có quá trình:
+ Cho e : Fe → Fe+3 + 3e
Cu → Cu2+ + 2e
+ Nhận e: S+6 + 2e → S+4
O + 2e → O-2
Theo DLBT e có: 3x + 2z = 2.0,0225 + 2y mX= 56x + 16y +64z=2,44
m muối = mFe2(SO4)3 + mCuSO4 = 200x + 160z= 6,6
Giải hệ ta được z= 0,01mol => mCu(X)= 0,64g => m(FexOy)=1,8g
=>%mFexOy= 73,77%
=>B

Coi oxit gồm $Fe(x\ mol) ; O(y\ mol)$
Ta có : 56x + 16y = 20,88(1)$
$n_{SO_2} = 0,145(mol)$
Bảo toàn electron : $3x = 2y + 0,145.2(2)$
Từ (1)(2) suy ra x = 0,29 ; y = 0,29$
$n_{Fe} : n_O = 0,29 : 0,29 = 1 : 1$
Do đó, oxit là $FeO$
$n_{Fe_2(SO_4)_3} = \dfrac{1}{2}n_{Fe} = 0,145(mol)$
$m_{Fe_2(SO_4)_3} = 0,145.400 = 58(gam)$

Đáp án A
Gọi số mol Fe là a; số mol O là b; số mol Cu là c
Khi đó 56a + 16b +64c = 2,44
Bảo toàn e có 3a + 2c =2b + 0,045
Khối lượng muối sunfat là 200a + 160c = 6,6
→ a = b = 0,025; c = 0,01

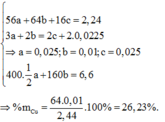

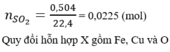
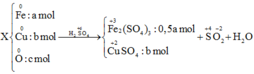
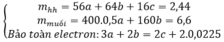
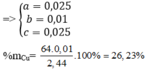
Coi hỗn hợp gồm : $Fe(a\ mol) ; O(b\ mol) ; Cu(c\ mol)$
Ta có : $56a + 16b + 64c = 2,44(1)$
$n_{SO_2} = \dfrac{0,504}{22,4} = 0,0225(mol)$
Bảo toàn electron : $3n_{Fe} + 2n_{Cu} = 2n_O + 2n_{SO_2}$
$\Rightarrow 3a + 2c = 2b + 0,0225.2(2)$
$n_{Fe_2(SO_4)_3} = 0,5a(mol)$
$n_{CuSO_4} = c(mol)$
$\Rightarrow m_{muối} =0,5a.400 + 160c = 6,6(3)$
Từ (1)(2)(3) suy ra a = 0,025 ; b = 0,025 ; c = 0,01
$\%m_{Cu} = \dfrac{0,01.64}{2,44}.100\% = 26,23\%$
$n_{Fe} : n_O = 0,025 : 0,025 = 1 : 1$
Suy ra CT của oxit là $FeO$
Coi hỗn hợp X gồm các nguyên tố Fe (x mol) , O (y mol) và Cu (z mol).
=> Hai muối sunfat là Fe2(SO4)3 (\(\dfrac{x}{2}\) mol) và CuSO4 (z mol)
Ta có :
\(\left\{{}\begin{matrix}56x+16y+64z=2,44\\Bt\left(e\right):3x-2y+2z=\dfrac{2.0,504}{22,4}\\\dfrac{400x}{2}+160z=6,6\end{matrix}\right.\)
=>x=y=0,025, z=0,01
=>%Cu=\(\dfrac{0,01.64}{2,44}100\%=26,23\%\)