đốt cháy 200ml hơi 1 hợp chất hữu cơ X chứa C, H , O trong 900ml O2 , thể tích hỗn hợp khí thu đc là 1,3 lít . Sau khi ngưng tụ hơi nc chỉ còn 700ml . Tiếp theo cho qua dd KOH dư chỉ còn 100ml khí bay ra . Các thể tích khí đo ở cùng điều kiện nhiệt độ , áp suất . CTPT của Y là

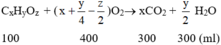

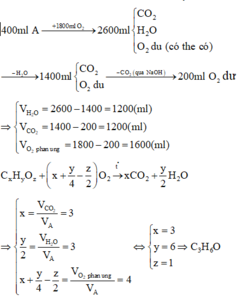
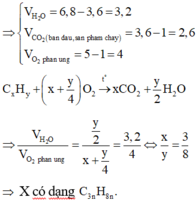
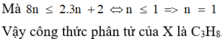
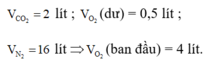
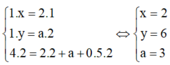
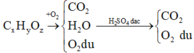
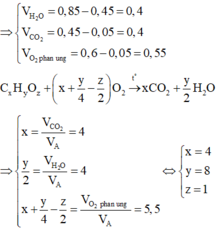
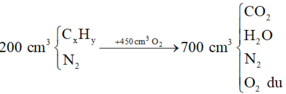
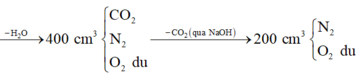
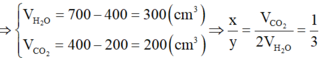
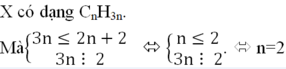
100ml khí bay ra là O2
=> VO2 (phản ứng) = 900 - 100 = 800 (ml)
VH2O = 1300 - 700 = 600 (ml)
VCO2 = 700 - 100 = 600 (ml)
=> \(V_X:V_{O_2}:V_{CO_2}:V_{H_2O}=200:800:600:600=1:4:3:3\)
Vì tỉ lệ thể tích cũng là tỉ lệ mol nên ta giả sử có: \(\left\{{}\begin{matrix}n_X=1\left(mol\right)\\n_{O_2\left(pư\right)}=4\left(mol\right)\\n_{H_2O}=3\left(mol\right)\\n_{CO_2}=3\left(mol\right)\end{matrix}\right.\)
Theo BTNT: \(\left\{{}\begin{matrix}n_C=n_{CO_2}=3\left(mol\right)\\n_H=2n_{H_2O}=6\left(mol\right)\\n_{O\left(X\right)}=2n_{CO_2}+n_{H_2O}-2n_{O_2}=1\left(mol\right)\end{matrix}\right.\)
=> X là `C_3H_6O`