cho 3.79 g hỗn hợp gồm zn và al tác dụng với dd h2so4 4.9% vừa đủ sau phản ứng thu được 0.896 lít khí ( ở 0 độ và 2 atm) và dung dịch X
a tính % khối lượng của mỗi kim loại trong hỗn hợp ban đầu
b tính khối lượng dd H2so4 đã dùng
c tính nống độ % của dung dịch A

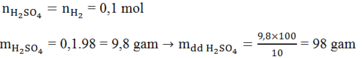
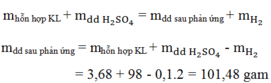

a) Gọi $n_{Zn} = a(mol) ; n_{Al} = b(mol) \Rightarrow 65a + 27b = 3,79(1)$
$Zn + H_2SO_4 \to ZnSO_4 + H_2$
$2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2$
Theo PTHH : $n_{H_2} = a + 1,5b = \dfrac{2.0,896}{0,082(273 + 0)} = 0,08(2)$
Từ (1)(2) suy ra a = 0,05 ; b = 0,02
$\%m_{Zn} = \dfrac{0,05.65}{3,79}.100\% = 85,75\%$
$\%m_{Al} = 100\% - 85,75\% = 14,25\%$
b) $n_{H_2SO_4} = n_{H_2} = 0,08(mol)$
$\Rightarrow m_{dd\ H_2SO_4} =\dfrac{0,08.98}{4,9\%} = 160(gam)$
c) $m_{dd\ A} = 3,79 + 160 - 0,08.2 = 163,63(gam)$
$C\%_{ZnSO_4} = \dfrac{0,05.161}{163,63}.100\% = 4,92\%$
$C\%_{Al_2(SO_4)_3} = \dfrac{0,01.342}{163,63}.100\% = 2,09\%$
1,5 ở đâu z anh