Hòa tan 4,59 gam Al bằng dung dịch HNO3 thu được hỗn hợp khí NO và N2O có tỉ khối hơi đối với hiđro bằng 16,75. Tính thể tích của NO và N2O
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
G o i n N O = a n N 2 O = b
Có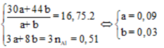
Vậy V N O = 2 , 016 ( l í t ) V N 2 O = 0 , 672 ( l í t )

Chọn B
Ta có: n A l = 0 , 17 (mol). Gọi = x mol, = y mol
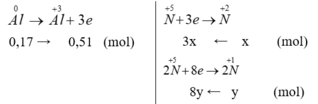
Bảo toàn số mol electron: 3x + 8y = 0,51 (1)
Mặt khác:
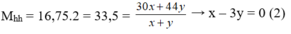
Giải (1) và (2) ta có: x = 0,09 (mol); y = 0,03 (mol)
⇒ V N O = 0 , 09 . 22 , 4 = 2 , 016 ( l ) , V N O 2 0 , 672 ( l )

Đáp án B
n A l = 0 , 17 g ọ i n N O = a n N 2 O = b c ó M ¯ = 30 a + 44 b a + b = 16 , 75 . 2 < = > a = 3 b ( 1 ) q u á t r ì n h n h ư ờ n g e :
A l o → A l + 3 + 3 e
Quá trình nhận e:

Từ (1) và (2)
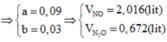

\(n_{Al}=0,17\left(mol\right)\)
Gọi số mol của NO, N2O là x và y
\(\dfrac{x}{y}=\dfrac{10,5}{3,5}=3\Rightarrow x=3y\left(1\right)\)
\(Al^0-3e->Al^{+3}\)
0,17......0,51
\(N^{+5}-+3e->N^{+2}O\)
3x.............x
\(2N^{+5}-+8e->N^{+1}_2O\)
8y...........y
Bảo toàn e
\(3x+8y=0,51\left(2\right)\)
Giai (1) (2) => x=0,09 y=0,03
\(V_{NO}=0,09.22,4=2,016\left(l\right)\)
\(V_{N2O}=0,03.22,4=0,672\left(l\right)\)

\(n_{NO}=a\left(mol\right),n_{N_2O}=b\left(mol\right)\)
\(n_{Al}=\dfrac{4.5}{27}=\dfrac{1}{6}\left(mol\right)\)
Bảo toàn e :
\(3a+8b=\dfrac{1}{6}\cdot3=0.5\left(1\right)\)
\(\overline{M}=16.75\cdot2=33.5\left(g\text{/}mol\right)\)
\(\Rightarrow\dfrac{30a+44b}{a+b}=33.5\)
\(\Rightarrow3.5a-10.5b=0\left(2\right)\)
\(\left(1\right),\left(2\right):a=\dfrac{3}{34},b=\dfrac{1}{34}\)
\(V=\dfrac{3}{34}\cdot22.4=1.98\left(l\right)\)
\(V_1=\dfrac{1}{34}\cdot22.4=0.66\left(l\right)\)
Gọi $n_{NO} = a(mol) ; n_{N_2O} = b(mol)$
Ta có :
\(\dfrac{30a+44b}{a+b}=16,75.2\left(1\right)\)
$n_{Al} = \dfrac{4,59}{27} = 0,17(mol)$
Bảo toàn electron : $3n_{Al} = 3n_{NO} + 8n_{N_2O}$
$\Rightarrow 3a + 8b = 0,17.3(2)$
Từ (1)(2) suy ra a = 0,09 ; b = 0,03
$V_{NO} = 0,09.22,4 = 2,016(lít)$
$V_{N_2O} = 0,03.22,4 = 0,672(lít)$
\(\overline{M}_{NO,N_2O}=16,75.2=33,5\left(g/mol\right)\)
Theo sơ đồ đường chéo:
\(\dfrac{n_{NO}}{n_{N_2O}}=\dfrac{44-33,5}{33,5-30}=\dfrac{3}{1}\)
Gọi \(n_{N_2O}=x\left(mol\right)\Rightarrow n_{NO}=3x\left(mol\right)\)
\(n_{Al}=\dfrac{4,59}{27}=0,17\left(mol\right)\)
Quá trình oxi hoá - khử:
\(Al^0-3e\rightarrow Al^{+3}\\ 2N^{+5}+8e\rightarrow2N^{+1}\\ N^{+5}+3e\rightarrow N^{+2}\)
BTe: \(3n_{Al}=8n_{N_2O}+3n_{NO}\)
=> 8x + 3.3x = 0,17.3
=> x = 0,03
=> \(\left\{{}\begin{matrix}V_{N_2O}=0,03.22,4=0,672\left(l\right)\\V_{NO}=0,03.3.22,4=2,016\left(mol\right)\end{matrix}\right.\)