Bài 2 :Nguyên tử R có tổng ba loại hạt là 24.Số hạt mang điện gấp 2 lần số hạt không mang điện .
a.Tìm số lượng mỗi loại hạt ?
b.Tìm khối lượng nguyên tử R?
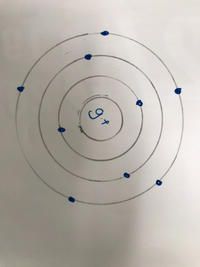
c. Vẽ sơ đồ cấu tạo nguyên tử R (tên nguyên tố R) ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)PTKX = 32 (đvC) => X là lưu huỳnh
=> X có 16 proton , 16 electron
Do nguyên tử khối của 1 chất = số p + số n của chất đó
=> X có : 32 - 16 = 16 (notron)
b) lớp 1 có 2e , lớp 2 có 8e , lớp 3 có 6e

Ta có p + e + n = 40.
Mà p = e => 2p + n = 40
Mặt khác, số hạt không mang điện (n) là 12 => n = 12
=> 2p = 40 - 12 = 28
=> p = 14
Vậy p = e = 14
n = 12

a) Gọi p, e, n lần lượt là số P, E, N của R.
Theo đề ta có p + e + n = 2p + n = 115 và p + e = 2p = 1,556n (vì p = e)
Suy ra p + e + n = 1,556n + n = 2,556n = 115
Hay \(n=\dfrac{115}{2,556}\approx45\)
Suy ra p + e + n = 2p + 45 = 2e + 45 = 115
Hay \(p=e=\dfrac{115-45}{2}=35\)
Vậy số hạt n, p, e của R lần lượt là 45 hạt, 35 hạt, 35 hạt.
b) Vì R có 35 e nên số hiệu nguyên tử của R là 35. Vậy R là nguyên tố hóa học thứ 35 của bảng tuần hoàn nguyên tố hóa học.
Tra bảng ta được R là Bromine.

a. Gọi số hạt của hạt P, E, N lần lượt là x, y, zTa có hệ phương trình:
x + y + z = 115 (1)
x + y = 1,556z (2)
Từ (1) và (2), suy ra:
z = (115 - y - x)/3 và x + y = 1,556(115 - y - x)/3
=> 3x + 3y = 1,556(115 - y - x)
=> 3x + 3y = 179180 - 1556x - 1556y
=> 4x + 4y = 179180
=> x + y = 44.795
Thay x + y = 44.795 vào (2), ta có z = 23.205
Vậy số hạt của hạt P, E, N lần lượt là x = 8.652, y = 36.143, z = 23.205
b. Ta biết rằng nguyên tử R có số hạt là 115, vậy ta có thể suy ra nguyên tử R là hợp phần của các nguyên tử có số hạt tương ứng như sau:
- Nguyên tử P có số hạt là 8
- Nguyên tử E có số hạt là 36
- Nguyên tử N có số hạt là 23
Vậy nguyên tử R là hợp phần của các nguyên tử P, E, N.

Tổng các loại hạt là 28 hạt
\(2p+n=28\left(1\right)\)
Số hạt mang điện nhiều hơn số hạt không mang điện là 8 hạt.
\(2p-n=8\left(2\right)\)
\(\left(1\right),\left(2\right):p=e=9.n=10\)
\(M=p+n=9+10=19\left(đvc\right)\)

a) Có \(\left\{{}\begin{matrix}p+n+e=2p+n=60\\p=n\end{matrix}\right.=>\left\{{}\begin{matrix}p=e=20\\n=20\end{matrix}\right.\)
=> R là Ca
b)
Cấu hình của Ca: 1s22s22p63s23p64s2
Có 20e => Ca nằm ở ô thứ 20
Có 4 lớp e => Ca thuộc chu kì 4
Có 2e lớp ngoài cùng => Ca thuộc nhóm IIA
c)
Nguyên tử Ca nhường 2e để đạt đến cấu hình bền của khí hiếm, tạo ra ion Ca2+
Cấu hình ion Ca2+ : 1s22s22p63s23p6
d) \(n_{O_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: 2Ca + O2 --to--> 2CaO
_____0,4<--0,2
=> mCaO = 0,4.40 = 16 (g)
a) Ta có :
$2p + n = 24$
mà : $2p = 2n$
Suy ra : $p = n = 8$
Nguyên tử R có 8 hạt proton, 8 hạt electron, 8 hạt notron
b)
$M_R = p + n = 16(u)$
$\Rightarrow m_R = 16.1,6605.10^{-27} = 26,568.10^{-27}(kg)$
c)
Tên nguyên tố : Oxi