Câu 1. Khi nguyên tử nhường hoặc nhận electron sẽ tạo thành
A. phân tử. B. ion. C. cation. D. anion.
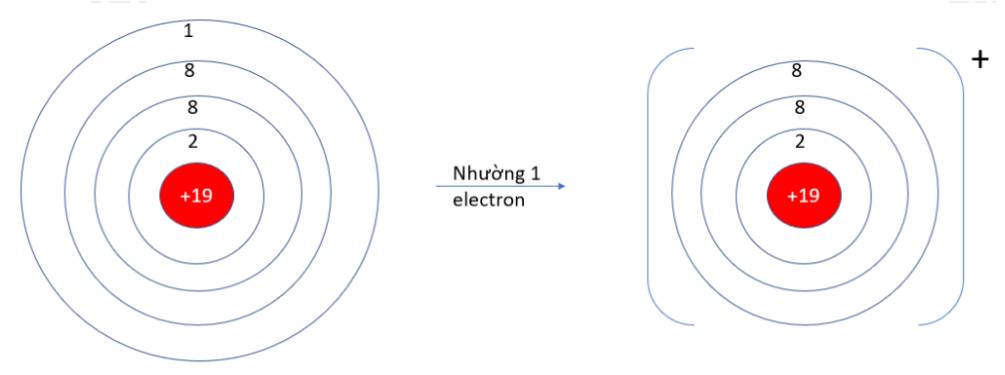
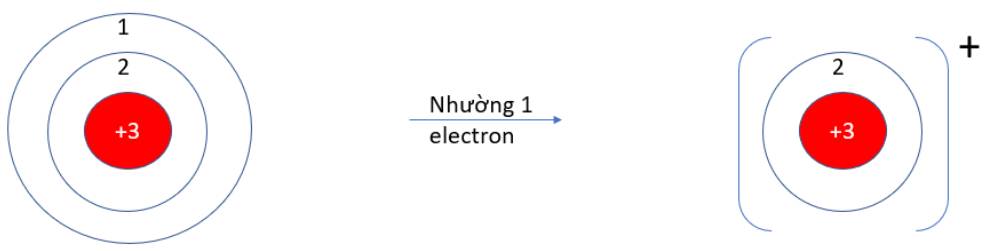
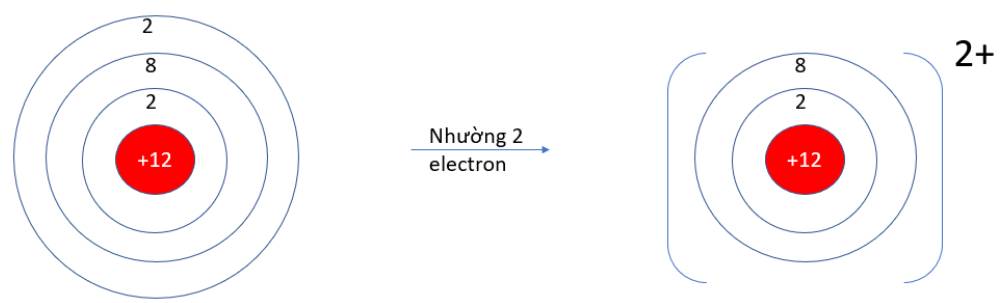
Câu 2. Khi nguyên tử nhường electron sẽ tạo thành
A. phân tử. B. ion. C. cation. D. anion.
Câu 3. Khi nguyên tử nhận electron sẽ tạo thành
A. phân tử. B. ion. C. cation. D. anion.
Câu 4. Nguyên tử của nguyên tố oxi có 6 electron ở lớp ngoài cùng, khi tham gia liên kết với các nguyên tố khác, oxi có xu hướng:
A. nhận thêm 1 electron. B. nhường đi 2 electron.
C. nhận thêm 2 electron. D. nhường đi 6 electron.




Câu 1 : B
Câu 2 : C
Nguyên tử bớt đi electron thì có điện tích dương
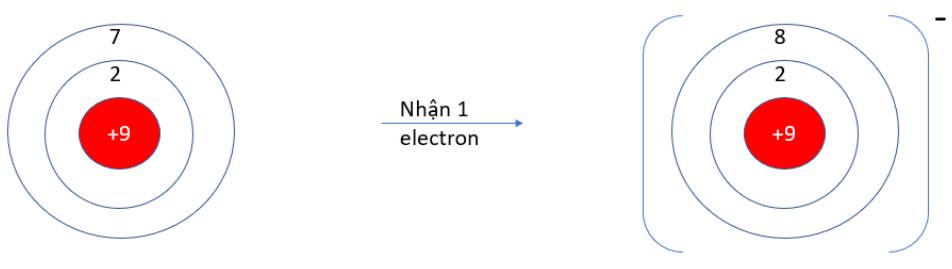
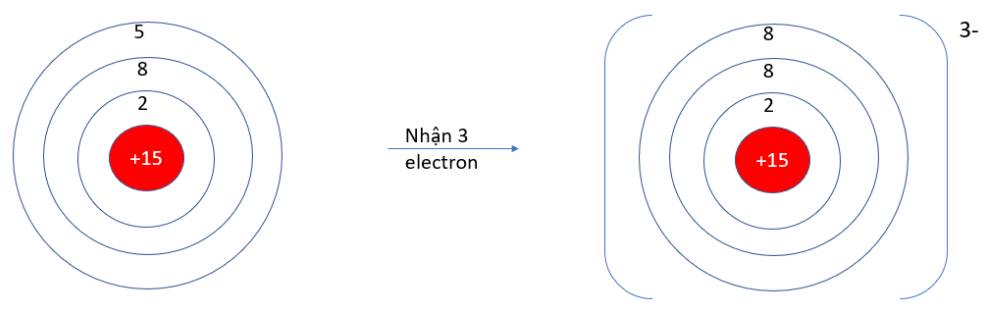
Câu 3 : D
Nguyên tử nhận thêm electron thì có điện tích âm
Câu 4 : C
$O^0 + 2e \to O^{-2}$