Lấy 1 lượng vừa đủ nhôm oxit tác dụng với 300ml H2SO4 0,5M
a)Khối lượng nhôm oxit đã phản ứng
b)Khối lượng muối đã tạo thành
c) Cũng lượng oxit nhôm trên cần bao nhiêu ml 3M
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Phương trình hóa học của phản ứng:
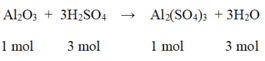
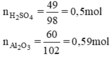
So sánh tỉ lệ 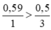 → Vậy Al2O3 dư
→ Vậy Al2O3 dư
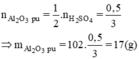
mAl2O3 (dư) = 60 - 17 = 43(g)

\(n_{Al2O3}=\dfrac{20,4}{102}=0,2\left(mol\right)\)
Pt : \(Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O|\)
1 3 1 3
0,2 0,6 0,2
\(n_{H2SO4}=\dfrac{0,2.3}{1}=0,6\left(mol\right)\)
⇒ \(m_{H2SO4}=0,6.98=58,8\left(g\right)\)
\(n_{Al2\left(SO4\right)3}=\dfrac{0,6.1}{3}=0,2\left(mol\right)\)
⇒ \(m_{Al2\left(SO4\right)3}=0,2.342=68,4\left(g\right)\)
Chúc bạn học tốt

Làm gộp cả phần a và b
Ta có: \(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{O_2}=0,15mol\\n_{Al_2O_3}=0,1mol\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}V_{O_2}=0,15\cdot22,4=3,36\left(l\right)\\m_{Al_2O_3}=0,1\cdot102=10,2\left(g\right)\end{matrix}\right.\)

Ta có: m dd H2SO4 = D.V = 1,5.200 = 300 (g)
\(\Rightarrow m_{H_2SO_4}=m_{ddH_2SO_4}.C\%=300.9,8\%=29,4\left(g\right)\)
\(\Rightarrow n_{H_2SO_4}=\dfrac{m}{M}=\dfrac{29,4}{98}=0,3\left(mol\right)\)
PT: \(Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O\)
_____0,1_______0,3______0,1 (mol)
a, \(m_{Al_2O_3}=n.M=0,1.102=10,2\left(g\right)\)
b, \(m_{Al_2\left(SO_4\right)_3}=n.M=0,1.342=34,2\left(g\right)\)
Bạn tham khảo nhé!

\(a,PTHH:4Al+3O_2\rightarrow^{t^o}2Al_2O_3\\ b,n_{Al_2O_3}=\dfrac{40,8}{102}=0,4\left(mol\right)\\ \Rightarrow n_{Al}=2n_{Al_2O_3}=0,8\left(mol\right)\\ \Rightarrow m_{Al}=0,8\cdot27=21,6\left(g\right)\\ b,n_{O_2}=\dfrac{3}{2}n_{Al_2O_3}=0,6\left(mol\right)\\ \Rightarrow V_{O_2\left(đktc\right)}=0,6\cdot22,4=13,44\left(l\right)\)

1)
a, \(n_{Al}=\dfrac{15,3}{102}=0,15\left(mol\right)\)
PTHH: Al2O3 + 6HCl → 2AlCl3 + 3H2O
Mol: 0,15 0,9 0,3
\(m_{ddHCl}=\dfrac{0,9.36,5.100}{20}=164,25\left(g\right)\)
b, mdd sau pứ = 15,3 + 164,25 = 179,55 (g)
c, \(C\%_{ddAlCl_3}=\dfrac{0,3.133,5.100\%}{179,55}=22,31\%\)
2)
a, \(m_{HCl}=54,75.20\%=10,95\left(g\right)\Rightarrow n_{HCl}=\dfrac{10,95}{36,5}=0,3\left(mol\right)\)
PTHH: Al2O3 + 6HCl → 2AlCl3 + 3H2O
Mol: 0,05 0,3 0,1
\(m_{Al_2O_3}=0,05.102=5,1\left(g\right)\)
b, mdd sau pứ = 5,1 + 54,75 = 59,85 (g)
\(C\%_{ddAlCl_3}=\dfrac{0,1.133,5.100\%}{59,85}=22,31\%\)
\(n_{H_2SO_4}=0,5.0,3=0,15\left(mol\right)\\ pthh:Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O\)
0,05 0,15 0,05
\(m_{Al_2O_3}=102.0,05=5,1\left(g\right)\\ m_{Al_2\left(SO_4\right)_3}=342.0,05=17,1\left(g\right)\\ n_{H_2SO_4}=n_{Al_2O_3}=0,15\left(mol\right)\\ C_{M\left(H_2SO_4\right)}=\dfrac{0,15}{3}=0,05\left(l\right)hay50\left(ml\right)\)
\(n_{H_2SO_4}=0,5.0,3=0,15\left(mol\right)\\ pthh:Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O\)
0,05 0,15 0,05
\(m_{Al_2O_3}=102.0,05=5,1\left(g\right)\\ m_{Al_2\left(SO_4\right)_3}=342.0,05=17,1\left(g\right)\)
\(n_{HCl}=3n_{Al}=0,15\left(mol\right)\\ C_{M\left(HCl\right)}=\dfrac{0,15}{3}=0,05\left(l\right)hay50ml\)