Cho 6,5 gam Zinc (Zn) tác dụng vừa đủ với 100ml dung dịch hydrochloric acid (HCl) thu được V lít khí hydrogen (H2) ở đktc
a) Viết phương trình phản ứng xảy ra
b) Tính giá trị V và khối lượng muối thu được sau phản ứng
c) Tính nồng độ mol/lít của dung dịch acid đã dùng
d) Dẫn toàn bộ lượng khí hydrogen thu được ở trên đi qua 12 gam bột CuO đun nóng. Tính khối lượng chất rắn thu được sau phản ứng


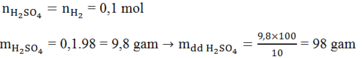
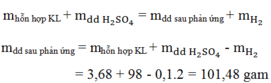
\(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\\ pthh:Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,2 0,1 0,1
\(V_{H_2}=0,1.22,4=2,24l\\ m_{ZnCl_2}=0,1.136=13,6g\\ C_{M\left(HCl\right)}=\dfrac{0,2}{0,1}=2M\\ n_{CuO}=\dfrac{12}{80}=0,15\left(mol\right)\\ pthh:CuO+H_2\underrightarrow{t^o}Cu+H_2O\\ LTL:0,15>0,1\)
=> CuO dư
\(n_{CuO\left(p\text{ư}\right)}=n_{Cu}=n_{H_2}=0,1\left(mol\right)\\ m_{cr}=\left(0,05.80\right)+\left(0,1.64\right)=10,4g\)