Hòa tan 6 gam kim loại M vào dd hcm dư , sau khi phản ứng kết thúc thấy dd tăng 5,5 gam . Vậy M là kim loại nào
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Câu 1:
2M+nCuSO4\(\rightarrow\)M2(SO4)n+nCu
2M+nFeSO4\(\rightarrow\)M2(SO4)n+nFe
- Gọi a là số mol của M
- Độ tăng khối lượng PTHH1:
64na/2-Ma=20 hay(32n-M).a=20
- Độ tăng khối lượng PTHH2:
56.na/2-Ma=16 hay (28n-M)a=16
Lập tỉ số ta được:\(\dfrac{32n-M}{28n-M}=\dfrac{20}{16}=1,25\)
32n-M=35n-1,25M hay 0,25M=3n hay M=12n
n=1\(\rightarrow\)M=12(loại)
n=2\(\rightarrow\)M=24(Mg)
n=3\(\rightarrow\)M=36(loại)
Câu 2:Gọi A là khối lượng thanh R ban đầu.
R+Cu(NO3)2\(\rightarrow\)R(NO3)2+Cu
R+Pb(NO3)2\(\rightarrow\)R(NO3)2+Pb
- Gọi số mol Cu(NO3)2 và Pb(NO3)2 là x mol
- Độ giảm thanh 1: \(\dfrac{\left(R-64\right)x}{A}.100=0,2\)
- Độ tăng thanh 2: \(\dfrac{\left(207-R\right)x}{A}.100=28,4\)
Lập tỉ số: \(\dfrac{207-R}{R-64}=\dfrac{28,4}{0,2}=142\)
207-R=142R-9088 hay 143R=9295 suy ra R=65(Zn)

Tham khảo:
Vì sau p/ư khối lượng dung dịch tăng 0,55g và trong quá trình phản ứng có giải phóng khí H2 nên
m\(_{H_2}\)= 6-5,5= 0,5g
=> n\(_{H_2}\)= 0,5:2= 0.25 mol
PTHH: R + 2HCl --> RCl(2) + H(2)
0,25 mol <-- 0,25 mol
=>MR= 6:0,25=24(g/mol)
vậy kl cần tìm là magie (Mg)

`MO + 2HCl -> MCl_2 + H_2O`
Theo PT: `n_(MO) = (n_(HCl))/2`
`<=> 8/(M_M +16) = (0,4)/2`
`<=> M_M = 24`
`=>M` là `Mg`.
\(MO+2HCl\rightarrow MCl_2+H_2O\)
Ta có : \(n_{MO}=\dfrac{1}{2}n_{HCl}=0,2\left(mol\right)\)
=> \(M_{MO}=\dfrac{8}{0,2}=40\)
=> M=24 (Mg)

\(a,Mg+H_2SO_4\rightarrow MgSO_4+H_2\\ 2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ m_{tăng}=m_{hhMg,Al}-m_{H_2}\\ \Leftrightarrow7=7,8-m_{H_2}\\ \Leftrightarrow m_{H_2}=0,8\left(g\right)\\ \Rightarrow n_{H_2}=\dfrac{0,8}{2}=0,4\left(mol\right)\\ Đặt:a=n_{Al}\left(mol\right);n_{Mg}=b\left(mol\right)\left(a,b>0\right)\\ \Rightarrow\left\{{}\begin{matrix}24b+27a=7,8\\b+1,5a=0,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\\m_{Mg}=24.0,1=2,4\left(g\right);m_{Al}=0,2.27=5,4\left(g\right)\\ \Rightarrow\%m_{Al}=\dfrac{0,2.27}{7,8}.100\approx69,231\%\\ \Rightarrow\%m_{Mg}\approx30,769\%\\ c,m_{muối}=m_{MgSO_4}+m_{Al_2\left(SO_4\right)_3}=120b+342.0,5a=120.0,1+342.0,5.0,2=46,2\left(g\right)\)

Đáp án C
Số mol H2 thu được là: n H 2 = 0 , 8 2 = 0 , 4 m o l
Gọi n là hóa trị của M
Phương trình hóa học:
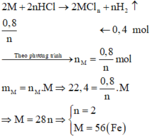
=> M là Fe

R + H2O -> ROH + 1/2 H2
nH2= 0,15(mol)
=> nROH=0,3(mol)
mROH= 6%.200=12(g)
=> M(ROH)= 12/0,3=40(g/mol)
Mà: M(ROH)=M(R)+17
=>M(R)+17=40
=>M(R)=23(g/mol) => R là Natri (Na=23)
mtăng = mM - mH2 = 5.5 (g)
=> mH2 = 6 - 5.5 = 0.5 (g)
nH2 = 0.5/2 = 0.25 (mol)
2M + 2nHCl => 2MCln + nH2
0.5/n.................................0.25
MM = 6/0.5/n = 12n
BL :
n = 2 => M = 24
M là : Mg
Em cảm ơn ạ