Cho 3.86 gam hỗn hợp fe và fes tác dụng với v (ml) dung dịch hcl 1M thu được 1.344 lít khí (dktc) tính V
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{hh.khí}=\dfrac{1,344}{22,4}=0,06\left(mol\right)\\ \rightarrow n_{HCl}=0,06.2=0,12\left(mol\right)\\ V_{HCl}=\dfrac{0,12}{1}=0,12\left(l\right)=120\left(ml\right)\)

Gọi số mol Al, Fe là a, b (mol)
=> 27a + 56b = 11,1 (1)
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
a----------------------->1,5a
Fe + 2HCl --> FeCl2 + H2
b------------------------>b
=> 1,5a + b = 0,3 (2)
(1)(2) => a = 0,1; b = 0,15
=> \(\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,1.27}{11,1}.100\%=24,32\%\\\%m_{Fe}=\dfrac{0,15.56}{11,1}.100\%=75,68\end{matrix}\right.\)

\(n_{hhkhí\left(H_2,H_2S\right)}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Gọi \(\left\{{}\begin{matrix}n_{Fe}=a\left(mol\right)\\n_{FeS}=b\left(mol\right)\end{matrix}\right.\)
PTHH:
Fe + 2HCl ---> FeCl2 + H2
a a
FeS + 2HCl ---> FeCl2 + H2S
b b
Hệ pt \(\left\{{}\begin{matrix}56a+88b=7,2\\a+b=0,1\end{matrix}\right.\Leftrightarrow a=b=0,05\left(mol\right)\)

nhh=0,11 mol
n PbS=0,1 mol
a) Phương trình hóa học của phản ứng:
Fe + 2HCl → FeCl2 + H2 (1)
FeS + 2HCl → FeCl2 + H2S (2)
H2S + Pb(NO3)2 → PbS + 2HNO3 (3)
b) Hỗn hợp khí thu được là H2 và H2S
Theo pt (3) ⇒ nH2S = nPbS = 0,1 mol
⇒ nH2 = nhh khí - nH2S = 0,11 – 0,1 = 0,01 mol
VH2 = 0,01 x 22,4 = 0,224l.
VH2S = 0,1 x 22,4 = 2,24l.
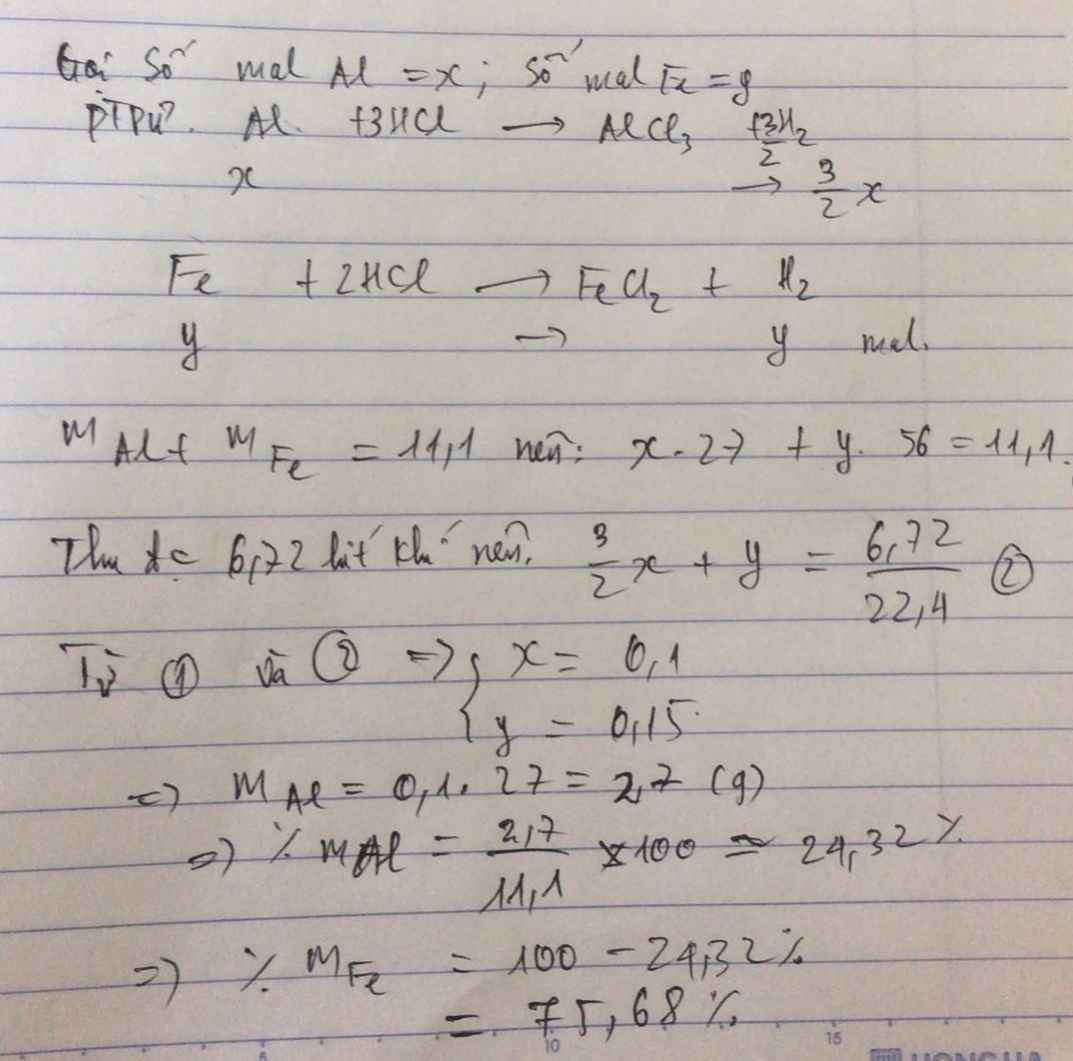
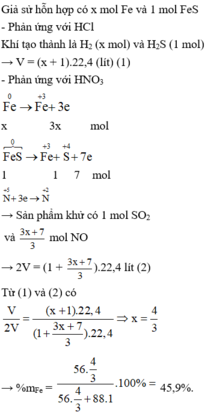
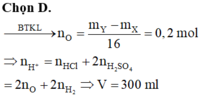
\(n_{hh.khí}=\dfrac{1,344}{22,4}=0,06\left(mol\right)\)
PTHH:
Fe + 2HCl ---> FeCl2 + H2
FeS + 2HCl ---> FeCl2 + H2S
Theo pthh: nHCl = 2nhh khí = 2.0,06 = 0,12 (mol)
=> Vdd HCl = \(\dfrac{0,12}{1}=0,12\left(l\right)=120\left(ml\right)\)