Cho thêm 40 gam H2O vào 20 gam dung dịch H2SO4 a% thu được dung dịch H2SO4 10% . Tìm giá trị của a
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


`a)`
`n_{SO_3}=0,005(mol)`
`m_{H_2SO_4\ 10\%}=10\%.a=0,1a(g)`
`SO_3+H_2O->H_2SO_4`
`0,005->0,005->0,005(mol)`
`->C\%_{H_2SO_4\ sau}={0,005.98+0,1a}/{0,4+a}.100=12,25`
`->a=19,6(g)`
`b)`
`n_{Ba(OH)_2}=0,01.0,5=0,005(mol)`
`n_{H_2SO_4}=0,005+{0,1.19,6}/{98}=0,025(mol)`
`n_{NaOH}=0,05.0,8=0,04(mol)`
`Ba(OH)_2+H_2SO_4->BaSO_4+2H_2O`
`0,005->0,005(mol)`
`->n_{H_2SO_4\ du}=0,025-0,005=0,02(mol)`
`2NaOH+H_2SO_4->Na_2SO_4+2H_2O`
Do `0,02={0,04}/2->` Pu hoàn toàn.
Theo PT : `n_{Na_2SO_4}=n_{H_2SO_4}=0,02(mol)`
`->m_{Na_2SO_4}=0,02.142=2,84<6,44`
`->X` là muối ngậm nước.
Đặt X là `Na_2SO_4.xH_2O`
Bảo toàn Na: `n_{Na_2SO_4.xH_2O}=n_{Na_2SO_4}=0,02(mol)`
`->M_{Na_2SO_4.xH_2O}={6,44}/{0,02}=322(g//mol)`
`->142+18x=322`
`->x=10`
`->X` là `Na_2SO_4.10H_2O`

\(C\%_{NaOH}=\dfrac{a}{a+40}=20\%\\ \Leftrightarrow a=10\left(g\right)\)

n CaCO 3 = 0 , 5 ⇒ n CO 3 2 - = 0 , 5
n H 2 SO 4 = 0 , 3 . 0 , 5 = 0 , 15 ⇒ n H + = 0 , 3 ; n SO 4 2 - = 0 , 15
Ta có: n CO 3 2 - > n H + => Chỉ xảy ra phản ứng: H + + CO 3 2 - → HCO 3 - và CO 3 2 - còn dư
Vậy dung dịch Y chứa 6 muối chỉ có thể là
Na2CO3; K2CO3; KHCO3; NaHCO3; Na2SO4; K2SO4
Trong Y chứa các anion: CO 3 2 - ( a mol ) ; HCO 3 - ( b mol ) ; SO 4 2 - ( 0 , 15 mol )
Khi thêm Ba(OH)2 dư vào dung dịch Y ta có các phản ứng:

Ta có a + b = n CO 3 2 - = 0 , 5 ⇒ m = 0 , 5 . 197 + 0 , 15 . 233 = 133 , 45 gam
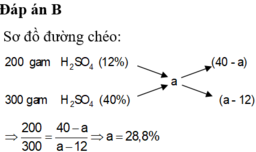
Đáp án C

Đáp án D.
![]()
![]()
Zn + H2SO4 → ZnSO4 + H2
0,1 → 0,1 → 0,1
H2SO4 + Ba(OH)2 → BaSO4 + 2H2O
0,3 → 0,3 → 0,4
ZnSO4 + Ba(OH)2 → BaSO4 + Zn(OH)2
0,1 0,25 → 0,1 → 0,1
Zn(OH)2 + Ba(OH)2 → BaZnO2 + 2H2O
0,1 0,15
Kết tủa thu được gồm 0,4 mol BaSO4: m = 0,4.233 = 93,2 gam
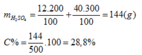
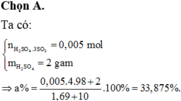

\(m_{H_2SO_4}=\dfrac{20.a}{100}=0,2a\left(g\right)\)
mdd sau khi thêm = 40 + 20 = 60 (g)
\(C\%_{dd.sau.khi.thêm}=\dfrac{0,2a}{60}.100\%=10\%\)
=> a = 30