Cho 2,24 lít khí CO, (đktc) vào 800ml dung dịch Ca(OH)2 0,1M thu được bao nhiêu gam muối
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(n_{NaOH}=0,4.0,4=0,16\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{n_{NaOH}}{n_{CO_2}}=\dfrac{0,16}{0,1}=1,6\)
=> Tạo ra muối Na2CO3 và NaHCO3
PTHH: 2NaOH + CO2 --> Na2CO3 + H2O
0,16--->0,08---->0,08
Na2CO3 + CO2 + H2O --> 2NaHCO3
0,02<---0,02------------->0,04
=> \(\left\{{}\begin{matrix}m_{Na_2CO_3}=\left(0,08-0,02\right).106=6,36\left(g\right)\\m_{NaHCO_3}=0,04.84=3,36\left(g\right)\end{matrix}\right.\)
=> mmuối = 6,36 + 3,36 = 9,72 (g)
\(n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ n_{NaOH}=0,4.0,4=0,16\left(mol\right)\)
\(T=\dfrac{0,16}{0,1}=1,6\rightarrow\) Tạo cả 2 muối
Gọi \(\left\{{}\begin{matrix}n_{Na_2CO_3}=a\left(mol\right)\\n_{NaHCO_3}=b\left(mol\right)\end{matrix}\right.\)
PTHH: 2NaOH + CO2 ---> Na2CO3 + H2O
2a a a
NaOH + CO2 ---> NaHCO3
b b b
Hệ pt: \(\left\{{}\begin{matrix}2a+b=0,16\\a+b=0,1\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,06\left(mol\right)\\b=0,04\left(mol\right)\end{matrix}\right.\)
=> mmuối = 0,06.106 + 0,04.84 = 9,72 (g)

Chọn A
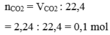
Theo bài ra ta có sau phản ứng chỉ thu được muối CaC O 3 do đó ta có phản ứng

1. Gọi V là thể tích của dung dịch Ca(OH)2
\(n_{CO_2}=0,01\left(mol\right);n_{Ca\left(OH\right)_2}=0,25V\left(mol\right)\Rightarrow n_{OH-}=0,5V\left(mol\right)\)
Ta có : \(T=\dfrac{n_{OH^-}}{n_{CO_2}}=\dfrac{0,5V}{0,1}=5V\)
Nếu T<1 \(\Leftrightarrow V< 0,2\)=> Chỉ tạo 1 muối Ca(HCO3)2 và CO2 dư
T=1 \(\Leftrightarrow V=0,2\) => Chỉ tạo 1 muối Ca(HCO3)2
1 < T < 2 \(\Leftrightarrow0,2< V< 0,4\)=> Tạo 2 muối Ca(HCO3)2 và CaCO3
T=2 \(\Leftrightarrow V=0,4\) => Chỉ tạo 1 muối CaCO3
T >2\(\Leftrightarrow V>0,4\) => Chỉ tạo 1 muối CaCO3 và Ca(OH)2 dư
2. \(n_{CO_2}=0,2\left(mol\right);n_{Ca\left(OH\right)_2}=\dfrac{4}{37}\Rightarrow n_{OH^-}=\dfrac{8}{37}\)
Lập T = \(\dfrac{\dfrac{8}{37}}{0,2}=1,08\) => Tạo 2 muối
Gọi x,y lần lượt là số mol Ca(HCO3)2 và CaCO3
\(\left\{{}\begin{matrix}2x+y=0,2\\x+y=\dfrac{4}{37}\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=\dfrac{17}{185}\\y=\dfrac{3}{185}\end{matrix}\right.\)
=> \(m_{muối}=\dfrac{17}{185}.162+\dfrac{3}{185}.100=16,51\left(g\right)\)

Đáp án C
Vì Ca(OH)2 dư ⇒ nCaCO3 = nCO2 = 0,1 mol
⇒ mCaCO3 = 0,1 × 100 = 10 gam ⇒ Chọn C

Đáp án D
nCO2 = 6,72: 22,4 = 0,3 mol
nCa(OH)2 = 0,25.1 = 0,25 mol => nOH = 2nCa(OH)2 = 0,5 mol
Ta thấy: nCO2 < nOH < 2nCO2
=> phản ứng tạo hỗn hợp muối HCO3 và CO3
=> nCO3 = nOH – nCO2 = 0,5 – 0,3 = 0,2 mol < nCa2+
=> nCaCO3 = nCO3 = 0,2 mol
=> mkết tủa = 0,2. 100 = 20g

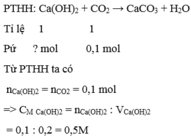
a/ PTHH: CO2 + Ca(OH)2 ===> CaCO3+ H2O
nCO2 = 2,24 / 22,4 = 0,1 mol
=> nCa(OH)2 = nCaCO3 = nCO2 = 0,1 mol
=> CM(CaOH)2 = 0,1 / 0,2 = 0,5M
b/ => mCaCO3 = 0,1 x 100 = 10 gam



\(n_{CO}=\dfrac{2,24}{22,4}=0,1mol\)
\(n_{Ca\left(OH\right)_2}=0,8\cdot0,1=0,08mol\)
\(CO+Ca\left(OH\right)_2\underrightarrow{t^o}CaCO_3+H_2\)
0,1 0,08 0,08
\(m_{muối}=m_{CaCO_3}=0,08\cdot100=8g\)
ko có muối vì khí td là CO