Đốt cháy 16,8 g sắt trong không khí
a) Tính thể tích không khí cần dùng (đkc), biết rằng thể tích khí oxi chiếm 1/5 thể tích không khí.
b) Tính khối lượng oxit tạo ra. Gọi tên oxit đó
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(3Fe+2O_2\rightarrow^{t^0}Fe_3O_4\)
3 : 2 : 1
0,3 : 0,2 : 0,1
\(n_{Fe}=\dfrac{m}{M}=\dfrac{16,8}{56}=0,3\left(mol\right)\)
a. \(V_{O_2\left(đktc\right)}=n.24,79=0,2.24,79=4,958\left(l\right)\)
\(V_{kk\left(đktc\right)}=V_{O_2\left(đktc\right)}.5=4,958.5=24,79\left(l\right)\)
b. \(m_{Fe_3O_4}=n.M=0,1.232=23,2\left(g\right)\)
-Tên oxit đó là oxit sắt từ (Iron (II,III) oxide)

$a\big)$
$n_{Fe}=\frac{16,8}{56}=0,3(mol)$
$3Fe+2O_2\xrightarrow{t^o}Fe_3O_4$
Theo PT: $n_{Fe_3O_4}=\frac{1}{3}n_{Fe}=0,1(mol)$
$\to m_{Fe_3O_4}=0,1.232=23,2(g)$
$b\big)$
Theo PT: $n_{O_2}=\frac{2}{3}n_{Fe}=0,2(mol)$
$\to V_{O_2}=0,2.22,4=4,48(l)$
$\to V_{kk}=4,48.5=22,4(l)$
$c\big)$
$2KMnO_4\xrightarrow{t^o}K_2MnO_4+MnO_2+O_2$
Theo PT: $n_{KMnO_4}=2n_{O_2}=0,4(mol)$
$\to m_{KMnO_4(dùng)}=\frac{0,4.158}{80\%}=79(g)$
a, \(n_{Fe}=\dfrac{16,8}{56}=0,3\left(mol\right)\)
PTHH: 3Fe + 2O2 ---to→ Fe3O4
Mol: 0,3 0,2 0,1
\(m_{Fe_3O_4}=0,1.232=23,2\left(g\right)\)
b, \(V_{O_2}=0,2.22,4=4,48\left(l\right)\Rightarrow V_{kk}=4,48.5=22,4\left(l\right)\)
c,
PTHH: 2KMnO4 ---to→ K2MnO4 + MnO2 + O2
Mol: 0,4 0,2
\(m_{KMnO_4\left(lt\right)}=0,4.158=63,2\left(g\right)\)
\(\Rightarrow m_{KMnO_4\left(tt\right)}=\dfrac{63,2}{80\%}=79\left(g\right)\)

a.b.
\(n_{Fe}=\dfrac{16,8}{56}=0,3mol\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
0,3 0,2 0,1 ( mol )
\(m_{Fe_3O_4}=0,1.232=23,2g\)
\(V_{O_2}=0,2.22,4=4,48l\)
\(V_{kk}=4,48.5=22,4l\)
c.
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
0,4 0,2 ( mol )
\(m_{KMnO_4}=\dfrac{0,4.158}{\left(100-20\right)\%}=79g\)
a/ Số mol Fe là : nFe = 16,8: 56 = 0,3 mol
PTPƯ:
3Fe + 2O2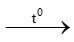 Fe3O4 (1)
Fe3O4 (1)
0,3 mol → 0,2mol → 0,1 mol
Từ (1) ta có số mol Fe3O4 = 0,1mol
→ m Fe3O4 = n.M = 0,1.232 = 23,2gam
b/ Từ (1) ta có số mol O2 đã dùng nO2 = 0,2 mol
Thể tích khí oxi đã dùng ở đktc: VO2 = n.22,4 = 0,2.22,4 = 4,48 lít
Thể tích không khí đã dùng: Vkk = 5. VO2= 5.4,48 = 22,4 lít.
c/ PTPƯ
2 KMnO4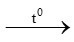 K2MnO4 + MnO2 + O2 (2)
K2MnO4 + MnO2 + O2 (2)
0,4444mol ← 0,222mol
Vì lượng Oxi thu được hao hụt 10% nên số mol O2 cần có là:
nO2 = 0,2mol.100/90 = 0.222 mol
Từ (2) ta có số mol KMnO4 = 0,444mol
Khối lượng KMnO4 bị nhiệt phân
mKMnO4 = n.M = 0,444.158 = 70.152 gam

a) nFe = 16,8/56 = 0,3 (mol)
PTHH: 3Fe + 2O2 -> (t°) Fe3O4
Mol: 0,3 ---> 0,2 ---> 0,1
mFe3O4 = 0,1 . 232 = 23,2 (g)
b) VO2 = 0,2 . 22,4 = 4,48 (l)
Vkk = 4,48 . 5 = 22,4 (l)
c) H = 100% - 20% = 80%
nO2 (LT) = 0,2 : 80% = 0,25 (mol)
PTHH: 2KMnO4 -> (t°) K2MnO4 + MnO2 + O2
nKMnO4 = 0,25 . 2 = 0,5 (mol)
mKMnO4 = 0,5 . 158 = 79 (g)

nMg = 7,2/24 = 0,3 (mol)
PTHH: 2Mg + O2 -> (t°) 2MgO
Mol: 0,3 ---> 0,15 ---> 0,3
VO2 = 0,15 . 22,4 = 3,36 (l)
Vkk = 3,36 . 5 = 16,8 (l)
mMgO = 0,3 . 40 = 12 (g)

a)
\(n_{Al}=\dfrac{13,5}{27}=0,5\left(mol\right)\)
PTHH: 4Al + 3O2 --to-- 2Al2O3
_____0,5-->0,375--->0,25
=> mAl2O3 = 0,25.102 = 25,5 (g)
b) VO2 = 0,375.22,4 = 8,4 (l)
=> Vkk = 8,4.5 = 42 (l)

\(n_{Fe}=\dfrac{1,68}{56}=0,03\left(mol\right)\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
0,03 0,02 0,01 ( mol )
\(m_{Fe_3O_4}=0,01.232=2,32\left(g\right)\)
\(V_{kk}=0,02.22,4.5=2,24\left(l\right)\)
\(2KClO_3\rightarrow\left(t^o\right)2KCl+3O_2\)
\(\dfrac{1}{75}\) 0,02 ( mol )
\(m_{KClO_3}=\dfrac{1}{75}.122,5=1,63\left(g\right)\)
a,nFe=1,68/56=0,03 mol
Ta có PTHH : 3Fe + 2O2 --> Fe3O4 (1) ( ở trên dấu --> có to nha )
Theo PTHH ta có :
nFe3O4=1/3nFe=1/3.0,03=0,01 mol
nO2=2/3nFe=2/3.0,03=0,02 mol
=>mFe3O4= 0,01.232=2,32g
=>Vkk=5.(0,02.22,4)=2,24 l
b, Ta có PTHH: 2KClO3 --> 2KCl + 3O2 (2) ( trên dấu --> vẫn có to )
Gọi x là số mol KClO3 cần dùng ( x > 0 )
Theo PTHH (3) và theo bài ra ta có PTHH sau:
2/3x=0,02
=> x=0,03 mol
=> mKClO3= 0,03.122,5= 3,675g
![]()

a)\(2Mg + O_2 \xrightarrow{t^o} 2MgO\)
b)
\(n_{Mg} = \dfrac{2,4}{24} = 0,1(mol)\)
Theo PTHH :
\(n_{O_2} = \dfrac{1}{2}n_{Mg} = 0,05(mol)\\ \Rightarrow V_{O_2} = 0,05.22,4 = 1,12(lít)\)
c)
\(n_{MgO} = n_{Mg} = 0,1(mol)\\ \Rightarrow m_{MgO} = 0,1.40 = 4(gam)\)
d)
\(V_{không\ khí} = 5V_{O_2} = 1,12.5 = 5,6(lít)\)
\(n_{Fe}=\dfrac{16,8}{56}=0,3mol\)
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
0,3 0,2 0,1
\(V_{O_2}=0,2\cdot22,4=4,48l\)
\(V_{kk}=5V_{O_2}=5\cdot4,48=22,4l\)
\(m_{O_2}=0,2\cdot32=6,4g\)