Dẫn 2.24 lít khí SO2 vào dd 250ml dd KOH 0,2 M sau phản ứng thu đc là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) Chất rắn không tan là Cu
=> m Cu = 19,2(gam)
n Mg = a(mol) ; n Fe = b(mol)
=> 24a + 56b = 32,8 -19,2 = 13,6(1)
$Mg + H_2SO_4 \to MgSO_4 + H_2$
$Fe + H_2SO_4 \to FeSO_4 + H_2$
n H2 = a + b = 6,72/22,4 = 0,3(2)
Từ (1)(2) suy ra a = 0,1 ; b = 0,2
%m Cu = 19,2/32,8 .100% = 58,54%
%m Mg = 0,1.24/32,8 .100% = 7,32%
%m Fe = 100% -58,54% -7,32% = 34,14%
b)
m dd A = 32,8 + 200 - 0,3.2 = 232,2(gam)
n MgSO4 = a = 0,1(mol)
n FeSO4 = b = 0,2(mol)
C% MgSO4 = 0,1.120/232,2 .100% = 5,17%
C% FeSO4 = 0,2.152/232,2 .100% = 13,09%

Số mol khí SO2 là 3,36/22,4=0,15 (mol).
a) Số mol NaOH là 0,2.2=0,4 (mol).
2<OH-/SO2=8/3, muối thu được là Na2SO3 (0,15 mol) có khối lượng 0,15.126=18,9 (g).
b) Số mol NaOH là 4/40=0,1 (mol).
OH-/SO2=2/3<1, muối thu được là NaHSO3 (0,1 mol) có khối lượng 0,1.104=10,4 (g).
c) Số mol KOH là 0,1.2=0,2 (mol).
1<OH-/SO2=4/3<2, muối thu được gồm K2SO3 (0,2-0,15=0,05 (mol)) và KHSO3 (0,15-0,05=0,1 (mol)) có khối lượng lần lượt là 0,05.158=7,9 (g) và 0,1.120=12 (g).

\(n_{SO_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
\(n_{KOH}=0,2.2=0,4\left(mol\right)\)
Xét \(\dfrac{n_{KOH}}{n_{SO_2}}=\dfrac{0,4}{0,6}=0,67\) => tạo ra muối KHSO3
PTHH: KOH + SO2 --> KHSO3
0,4------------>0,4
=> mKHSO3 = 0,4.120 = 48 (g)

\(n_{H_2}=\dfrac{0,56}{22,4}=0,025\left(mol\right)\)
\(n_{NaOH}=0,25.1=0,25\left(mol\right)\)
Cho X vào dung dịch `H_2SO_4` loãng:
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
0,025<-----------------------0,025
a. \(\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{56.0,025.100\%}{11,8}=11,86\%\\\%m_{Cu}=\dfrac{\left(11,8-0,025.56\right).100\%}{11,8}=88,14\%\end{matrix}\right.\)
b. \(n_{Cu}=\dfrac{11,8-0,025.56}{64}=0,1625\left(mol\right)\)
Cũng lượng X trên cho vào dung dịch `H_2SO_4` đặc nóng:
Giả sử Fe tác dụng hết với dung dịch \(H_2SO_{4.đn}\)
\(2Fe+6H_2SO_{4.đn}\rightarrow Fe_2\left(SO_4\right)_3+3SO_2+6H_2O\)
0,025----------------------------------->0,0375
\(Cu+2H_2SO_{4.đn}\rightarrow CuSO_4+SO_2+2H_2O\)
0,1625--------------------------->0,1625
\(\Sigma n_{SO_2}=0,0375+0,1625=0,2\left(mol\right)\)
Có: \(\dfrac{n_{NaOH}}{n_{SO_2}}=\dfrac{0,25}{0,2}=1,25\)
=> Phản ứng giữa `NaOH` và `SO_2` tạo muối axit trước (tỉ lệ 1:1)
\(SO_2+NaOH\rightarrow NaHSO_3\)
0,2---->0,2------->0,2
Xét \(\dfrac{0,2}{1}< \dfrac{0,25}{1}\Rightarrow\) NaOH dư.
\(n_{NaOH.dư}=0,25-0,2=0,05\left(mol\right)\)
\(NaOH+NaHSO_3\rightarrow Na_2SO_3+H_2O\)
0,05----->0,05---------->0,05
Xét \(\dfrac{0,05}{1}< \dfrac{0,2}{1}\Rightarrow NaHSO_3.dư\)
Sau phản ứng thu được: \(\left\{{}\begin{matrix}n_{NaHSO_3}=0,2-0,05=0,15\left(mol\right)\\n_{Na_2SO_3}=0,05\left(mol\right)\end{matrix}\right.\)
\(m_{muối}=0,15.104+0,05.126=21,9=m_{muối.thu.được.theo.đề}\)
=> Giả sử đúng.
\(\Rightarrow V=V_{SO_2}=0,2.22,4=4,48\left(l\right)\)

1.\(n_{CO_2}=\dfrac{V}{22,4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
\(n_{KOH}=CM.Vdd=2.0,46=0,92\left(mol\right)\)
PTHH:\(CO_2+2KOH\rightarrow K_2CO_3+H_2O\)
TPU: 0,2 0,92
PU: 0,2 0,4 0,2
SPU: 0 0,52 0,2
\(m_{K_2CO_3}=n.M=0,2.138=27,6\left(g\right)\)
2.\(n_{SO_2}=\dfrac{V}{22,4}=\dfrac{8,69}{22,4}=0,4\left(mol\right)\)
\(n_{NaOH}=CM.Vdd=2,5.0,2=0,5\left(mol\right)\)
PTHH:\(SO_2+2NaOH\rightarrow Na_2SO_3+H_2O\)
TPU: 0,4 0,5
PU: 0,25 0,5 0,25
SPU: 0,15 0 0,25
\(m_{Na_2SO_3}=n.M=0,25.126=31,5\left(g\right)\)

nCO2=0,075mol
do dư KOH nên tạo ra muối trung hòa
nNa2CO3=nCO2=0,075mol
-->Cm=0,3M
Bạn phài gthich rõ :
Xét k=nKOH/nCO2=0.25/0.075=3.33
Vì k>2 nên xr phản ứng tạo muối trung hòa và có KOH dư
=>nKOH dư=0.25-(2*0.075)=0.1(mol)
=>CM(KOH dư)= 0.1/0.25=0.4(mol)
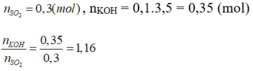
\(n_{SO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ n_{KOH}=0,2.0,25=0,05\left(mol\right)\\ T=\dfrac{0,05}{0,1}=0,5< 1\Rightarrow Tao.muối.axit\\ PTHH:KOH+SO_2\rightarrow KHSO_3\)