Có 2 hỗn hợp sau:
- Hỗn hợp A gồm 11,2 gam sắt và 3,2 gam đồng.
- Hỗn hợp B gồm 4,2 gam liti và 4,8 gam magie.
Hỏi:
- Hỗn hợp nào nặng hơn?
- Hỗn hợp nào chứa nhiều mol nguyên tử hơn?
- Hỗn hợp nào chứa nhiều nguyên tử hơn?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(Fe+S-t^0->FeS\\ n_{Fe}:n_S=\dfrac{11,2}{56}:\dfrac{4,8}{32}=0,2:0,15\Rightarrow Fe:dư\left(0,05mol\right)\\ Fe+2HCl->FeCl_2+H_2\\ FeS+2HCl->FeCl_2+H_2S\\ d_{\dfrac{B}{kk}}=\dfrac{\dfrac{0,05.2+0,15.34}{0,2}}{29}=0,89655\)

Đáp án A
X+ K (dư)
mbình tăng = mX – mH2 => mH2 = 12,2 – 11,9 = 0,3 gam
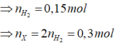
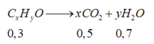
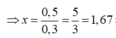
Số nguyên tử C là 1 và 3 => có 1 ancol là CH3OH
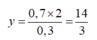
Gọi ancol còn lại là C3HaO
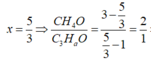
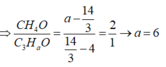
=> 2ancol là CH3OH và CH2=CH-CH2-OH

Chọn đáp án D
Câu này đề bài ra khá dở.Ta có thể suy ngay ra D vì:
+ Với A và B thì không thu được hai ancol có cùng số nguyên tử C.
+ Với C thì chỉ thu được 1 ancol vì C2H3OH không bền sẽ biến thành CH3CHO.
-
mA = 11,2 + 3,2 = 14,4 (g)
mB = 4,2 + 4,8 = 9 (g)
=> hh A nặng hơn hh B
-
\(n_A=\dfrac{11,2}{56}+\dfrac{3,2}{64}=0,25\left(mol\right)\)
\(n_B=\dfrac{4,2}{7}+\dfrac{4,8}{24}=0,8\left(mol\right)\)
=> hh B có chứa nhiều mol nguyên tử hơn hh A
-
Do hh B có chứa nhiều mol nguyên tử hơn hh A
=> hh B có chứa nhiều nguyên tử hơn hh A