Nêu pp phân biệt các chất rắn NaOH, Ba(OH)2; Mg(OH)2; Fe(OH)3
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a)
*Dùng quỳ tím
- Quỳ tím hóa đỏ: H2SO4 và MgCl2 (Nhóm 1)
- Quỳ tím hóa xanh: Ba(OH)2 và K2CO3 (Nhóm 2)
*Đổ dd BaCl2 vào từng nhóm
- Đối với nhóm 1
+) Xuất hiện kết tủa: H2SO4
PTHH: \(BaCl_2+H_2SO_4\rightarrow2HCl+BaSO_4\downarrow\)
+) Không hiện tượng: MgCl2
- Đối với nhóm 2
+) Xuất hiện kết tủa: K2CO3
PTHH: \(BaCl_2+K_2CO_3\rightarrow2KCl+BaCO_3\downarrow\)
+) Không hiện tượng: Ba(OH)2
b)
- Dùng quỳ tím
+) Quỳ tím hóa xanh: NaOH
+) Quỳ tím hóa đỏ: HCl
+) Quỳ tím không đổi màu: Na2SO4 và NaCl
- Đổ dd BaCl2 vào 2 dd còn lại
+) Xuất hiện kết tủa: Na2SO4
PTHH: \(BaCl_2+Na_2SO_4\rightarrow2NaCl+BaSO_4\downarrow\)
+) Không hiện tượng: NaCl
c) Giống phần a
d)
- Dung dịch màu vàng nâu: FeCl3
- Dùng quỳ tím
+) Quỳ tím không đổi màu: NaCl
+) Quỳ tím hóa đỏ: AgNO3 và HCl
- Đun nóng 2 dd còn lại
+) Xuất hiện chất rắn màu bạc và khí nâu đỏ: AgNO3
PTHH: \(AgNO_3\underrightarrow{t^o}Ag+NO_2\uparrow+\dfrac{1}{2}O_2\uparrow\)
+) Không hiện tượng: HCl

a)
| \(H_2SO_4\) | \(NaOH\) | \(Ba\left(OH\right)_2\) | \(HNO_3\) | |
| quỳ tím | đỏ | xanh | xanh | đỏ |
| \(BaCO_3\) | ↓trắng, | - | - | - |
| \(H_2SO_4\) | - | - | ↓trắng | - |
dán nhãn
b)
| \(HCl\) | \(Ca\left(OH\right)_2\) | \(KOH\) | \(Na_2SO_4\) | |
| quỳ tím | đỏ | xanh | xanh | - |
| \(CO_2\) | - | ↓trắng | - | - |
dán nhãn
b)
Lấy mỗi chất ra một ít và làm thí nghiệm sau:
- Nhúng quỳ tím vào các mẫu thử:
+ quỳ chuyển đỏ: HCl
+ quỳ chuyển xanh: \(Ca\left(OH\right)_2,KOH\) (I)
+ quỳ không chuyển màu: \(Na_2SO_4\)
- Cho dung dịch `Na_2CO_3` dư tác dụng với các chất ở nhóm (I):
+ có hiện tượng kết tủa trắng: \(Ca\left(OH\right)_2\)
\(Ca\left(OH\right)_2+Na_2CO_3\rightarrow CaCO_3+2NaOH\)
+ không hiện tượng: `KOH`

chọn B
Cho nước lần lượt vào các chất rắn. Chất rắn không tan là FeO, các chất còn lại tan
P 2 O 5 + 3 H 2 O → 2 H 3 PO 4
Nhúng quỳ tím vào các dung dịch thu được:
+) Dung dịch làm quỳ tím hóa đỏ là sản phẩm của P 2 O 5
+) Dung dịch làm quỳ tím hóa xanh là Ba ( OH ) 2
+) Dung dịch không có hiện tượng gì là NaNO 3

- Đổ nước vào từng chất rắn
+) Tan và tạo khí: Bari
PTHH: \(Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\uparrow\)
+) Không tan: FeO và Ag2O
- Sục khí CO vào từng chất rắn còn lại sau đó nung nóng rồi hút bằng nam châm
+) Chất rắn bị hút: FeO
PTHH: \(FeO+CO\underrightarrow{t^o}Fe+CO_2\uparrow\)
+) Không bị hút: Ag2O
PTHH: \(Ag_2O+CO\underrightarrow{t^o}2Ag+CO_2\uparrow\)

a)
- Đổ nước rồi khuấy đều
+) Tan: Na2O
+) Tan tạo dd vẩn đục: CaO
+) Không tan: MgO và CuO
- Đổ dd HCl vào 2 chất rắn còn lại
+) Tan và tạo dd màu xanh: CuO
PTHH: \(CuO+2HCl\rightarrow CuCl_2+H_2O\)
+) Tan: MgO

a.
- Trích mẫu thử.
- Cho quỳ tím vào các mẫu thử:
+ Nếu quyd tím hóa đỏ là HNO3 và H2SO4
+ Nếu quỳ tím không đổi màu là Ba(NO3)2
- Cho BaCl2 vào 2 mẫu thử còn lại:
+ Nếu có kết tủa trắng là H2SO4
\(H_2SO_4+BaCl_2--->BaSO_4\downarrow+2HCl\)
+ Nếu không có hiện tượng là HNO3
2HNO3 + BaCl2 ---> Ba(NO3)2 + 2HCl
b.
- Trích mẫu thử.
- Cho quỳ tím vào các mẫu thử:
+ Nếu quỳ tím hóa xanh là Ba(OH)2 và NaOH (1)
+ Nếu quỳ tím không đổi màu là NaCl và Na2SO4 (2)
- Cho H2SO4 vào nhóm (1):
+ Nếu có kết tủa trắng là Ba(OH)2
\(Ba\left(OH\right)_2+H_2SO_4--->BaSO_4\downarrow+2H_2O\)
+ Nếu không có hiện tượng là NaOH
2NaOH + H2SO4 ---> Na2SO4 + 2H2O
- Cho BaCl2 vào nhóm (2):
+ Nếu có kết tủa trắng là Na2SO4
\(Na_2SO_4+BaCl_2--->BaSO_4\downarrow+2NaCl\)
+ Nếu không có phản ứng là NaCl
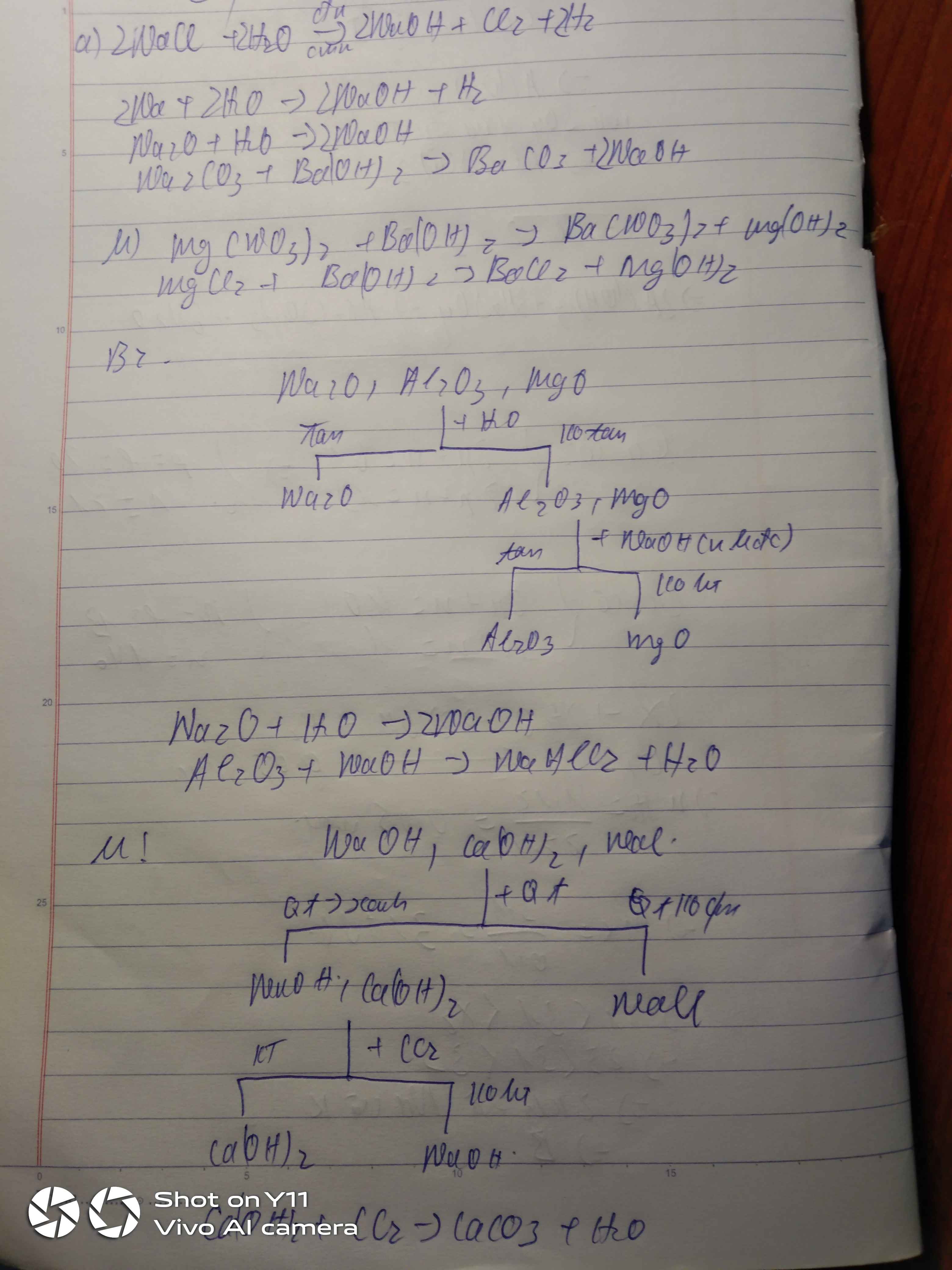
Nêu pp phân biệt các chất rắn NaOH, Ba(OH)2; Mg(OH)2; Fe(OH)3
Pb màu sắc :
-Fe(OH)3 màu vàng , nâu
-NaOH, Ba(OH)2dd ko màu
- Mg(OH)2 là kết tủa trắng
sau đó ta sục CO2
+ có kết tảu là Ba(OH)2
+còn lại là NaOH
Ba(OH)2+CO2-to>BaCO3+H2O
2NaOH+CO2->Na2CO3+H2O