cho 2,24 lít khí H2S vào 150ml dung dịch KOH 2m. Tính nồng độ các chất thu được
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{CO_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(n_{KOH}=0,15.1,5=0,225\left(mol\right)\)
Có: \(\dfrac{n_{KOH}}{n_{CO_2}}=0,45< 1\) → Pư tạo muối KHCO3 và CO2 dư.
PT: \(CO_2+KOH\rightarrow KHCO_3\)
____0,225_____0,225_____0,225 (mol)
\(\Rightarrow C_{M_{KHCO_3}}=\dfrac{0,225}{0,15}=1,5\left(M\right)\)

a) 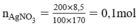
Phương trình hóa học của phản ứng:
HCl + AgNO3 → AgCl + HNO3
Theo pt nHCl = nAgCl = 0,1 mol
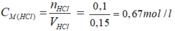
b) 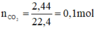
Phương trình hóa học của phản ứng:
HCl + NaHCO3 → NaCl + CO2↑ + H2O
Theo pt: nHCl = nCO2 = 0,1 mol ⇒ mHCl = 0,1. 36,5 = 3,65 g
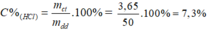

Ta có: \(n_{CO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
\(n_{KOH}=2.\dfrac{100}{1000}=0,2\left(mol\right)\)
Ta có: \(T=\dfrac{n_{KOH}}{n_{CO_2}}=\dfrac{0,2}{0,2}=1\)
Vậy, ta có PTHH:
\(CO_2+KOH--->KHCO_3\)
Theo PT: \(n_{KHCO_3}=n_{KOH}=0,2\left(mol\right)\)
Ta có: \(V_{dd_{KHCO_3}}=V_{dd_{KOH}}=100\left(ml\right)=0,1\left(lít\right)\)
\(\Rightarrow C_{M_{KHCO_3}}=\dfrac{0,2}{0,1}=2M\)

\(\left\{{}\begin{matrix}n_{H_2S}=\dfrac{2,464}{22,4}=0,11\left(mol\right)\\n_{NaOH}=0,05.2,5=0,125\left(mol\right)\end{matrix}\right.\)
Xét \(\dfrac{n_{NaOH}}{n_{H_2S}}=\dfrac{0,125}{0,11}=1,1\) => Tạo ra muối Na2S, NaHS
Gọi số mol NaOH phản ứng là để tạo muối Na2S, NaHS lần lượt là a, b (mol)
=> a + b = 0,125 (1)
PTHH: 2NaOH + H2S --> Na2S + 2H2O
a---->0,5a---->0,5a
NaOH + H2S --> NaHS + H2O
b---->b---------->b
=> 0,5a + b = 0,11 (2)
(1)(2) => a = 0,03 (mol); b = 0,095 (mol)
=> \(\left\{{}\begin{matrix}C_{M\left(Na_2S\right)}=\dfrac{0,5.0,03}{0,05}=0,3M\\C_{M\left(NaHS\right)}=\dfrac{0,095}{0,05}=1,9M\end{matrix}\right.\)

\(1,n_{SO_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\\ n_{NaOH}=1.0,3=0,3\left(mol\right)\)
\(T=\dfrac{0,3}{0,4}=0,75\rightarrow\)Tạo muối axit (NaHSO3) và SO2 dư
PTHH: NaOH + SO2 ---> NaHSO3
0,3------------------->0,3
\(C_{M\left(NaHSO_3\right)}=\dfrac{0,3}{0,3}=1M\)
\(2,n_{H_2S}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\ n_{NaOH}=0,2.2=0,4\left(mol\right)\)
\(T=\dfrac{0,4}{0,3}=\dfrac{4}{3}\rightarrow\)Tạo cả 2 muối (NaHS và Na2S)
PTHH:
2NaOH + H2S ---> Na2S + 2H2O
0,4--------->0,2------>0,2
Na2S + H2S ---> 2NaHS
0,1<------0,1------->0,2
\(\rightarrow\left\{{}\begin{matrix}C_{M\left(Na_2S\right)}=\dfrac{0,2-0,1}{0,2}=0,5M\\C_{M\left(NaHS\right)}=\dfrac{0,2}{0,2}=1M\end{matrix}\right.\)
1/ Số mol khí SO2 và NaOH lần lượt là 8,96:22,4=0,4 (mol) và 0,3.1=0,3 (mol). n\(OH^-\)/n\(SO_2\)=0,75<1, suy ra dung dịch thu được chỉ có muối NaHSO3 (0,3 mol).
Nồng độ mol cần tìm là CM \(\left(NaHSO_3\right)\)=0,3/0,3=1 (mol/l).
2/ Số mol khí H2S và NaOH là 6,72:22,4=0,3 (mol) và 0,2.2=0,4 (mol). n\(OH^-\)/n\(H_2S\)=4/3<2, suy ra dung dịch thu được chỉ có muối Na2S (0,2 mol).
Nồng độ mol cần tìm là CM \(\left(Na_2S\right)\)=0,2/0,2=1 (mol/l).

a)
Phương trình hóa học của phản ứng:
HCl + AgNO3 → AgCl + HNO3
Theo pt nHCl = nAgCl = 0,1 mol
b)
Phương trình hóa học của phản ứng:
HCl + NaHCO3 → NaCl + CO2↑ + H2O
Theo pt: nHCl = nCO2 = 0,1 mol ⇒ mHCl = 0,1. 36,5 = 3,65 g ( mình viết ko được rõ )
a.
mAgNO3 = (200.8,5%)/100 =17g
nAgNO3 = 17/170= 0,1 mol
để kết tủa hoàn toàn thì nAgNO3=nHCl = 0,1 mol
CHCl=0,1/0,15=2/3 (M)
b.
HCl + NaHCO3 =====> NaCl + CO2 + H2O
nCO2 = 0,1 mol=nHCl (theo pt)
mHCl =3,65 g
%CHCl = (3,65/50) .100% =7,3%

Bài 23 :
n BaCO3 = 0,1(mol) > n Ba(OH)2 = 0,15 mol
- TH1 : Ba(OH)2 dư
$Ba(OH)_2 + CO_2 \to BaCO_3 + H_2O$
n CO2 = n BaCO3 = 0,1(mol)
=> V = 0,1.22,4 = 2,24 lít
- TH1 : BaCO3 bị hòa tan một phần
$Ba(OH)_2 + CO_2 \to BaCO_3 + H_2O(1)$
$Ba(OH)_2 + 2CO_2 \to Ba(HCO_3)_2(2)$
n CO2(1) = n Ba(OH)2 (1) = n BaCO3 = 0,1(mol)
=> n Ba(OH)2 (2) = 0,15 - 0,1 = 0,05(mol)
=> n CO2 (2) = 2n Ba(OH)2 (2) = 0,1(mol)
=> V = (0,1 + 0,1).22,4 = 4,48 lít
nKOH = 0,15 . 2 = 0,3 (mol)
nH2S = 2,24/22,4 = 0,1 (mol)
PTHH: 2KOH + H2S -> K2S + 2H2O
LTL: 0,3/2 > 0,1 => KOH dư
nKOH (p/ư) = 0,1 . 2 = 0,2 (mol)
nKOH (dư) = 0,3 - 0,2 = 0,1 (mol)
nK2S = 0,1 (mol)
CMK2S = 0,1/0,15 = 0,66M
CMKOH = 0,1/0,15 = 0,66M