Dẫn 6,72 lít H2 qua 46,4 gam Fe3o4 sau khi phản ứng xảy ra hoàn toàn thu được m gam Fe Tính giá trị m ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


PTHH:
4H2+Fe3O4----->3Fe+4H2O
nH2=V/22,4=6,72/22,4=0,3mol
Theo PTHH:4molH2--->3molFe 0,3molH2->0,3.3/4=0,225molFe
mFe=nFe.M=0,225.56=12,6g
nO= nH2O= nH2= 0,3(mol)
m=m(oxit) - mO= 24- 0,3.16= 19,2(g)

\(a,PTHH:Fe_3O_4+4H_2\xrightarrow{t^o}3Fe+4H_2O\\ n_{H_2}=\dfrac{6,72}{22,4}=0,3(mol);n_{Fe_3O_4}=\dfrac{46,4}{232}=0,2(mol)\)
Vì \(\dfrac{n_{H_2}}{4}<\dfrac{n_{Fe_3O_4}}{1}\) nên \(Fe_3O_4\) dư
\(n_{Fe_3O_4(dư)}=0,2-\dfrac{0,3}{4}=0,125(mol)\\ \Rightarrow m_{Fe_3O_4(dư)}=0,125.232=29(g)\\ b,n_{Fe}=\dfrac{3}{4}n_{H_2}=0,225(mol)\\ \Rightarrow m_{Fe}=0,225.56=12,6(g)\)

a)\(n_{Fe}=\dfrac{16,8}{56}=0,3mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,3 0,3 0,3
\(V_{H_2}=0,3\cdot22,4=6,67l\)
\(m_{FeCl_3}=0,3\cdot127=38,1g\)
b)\(n_{Fe_2O_3}=\dfrac{18}{160}=0,1125mol\)
\(Fe_2O_3+3H_2\rightarrow2Fe+3H_2O\)
0,1125 0,3 0 0
0,1 0,3 0,2 0,3
0,0125 0 0,2 0,3
\(m_{Fe}=0,2\cdot56=11,2g\)

\(n_{CO\ dư} = a(mol) ; n_{CO_2} = b(mol)\\ \Rightarrow a + b = \dfrac{4,48}{22,4} = 0,2(1)\\ m_{khí} = 28a + 44b = 20,4.2.0,2 = 8,16(gam)(2)\\ (1)(2) \Rightarrow a = 0,04 ; b = 0,16\\ Fe_3O_4 + 4CO \xrightarrow{t^o} 3Fe + 4CO_2\\ n_{Fe_3O_4} = \dfrac{1}{4}n_{CO_2} = 0,04(mol)\\ m_{Fe_3O_4} = 0,04.232 = 9,28(gam)\)
Ta có: \(\Sigma n_{CO}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: \(Fe_3O_4+4CO\underrightarrow{t^o}3Fe+4CO_2\uparrow\)
Đặt \(n_{CO\left(p/ứ\right)}=a\left(mol\right)=n_{CO_2}\) \(\Rightarrow n_{CO\left(dư\right)}=0,2-a\)
\(\Rightarrow\dfrac{44a+28\left(0,2-a\right)}{a+\left(0,2-a\right)}=20,4\cdot2\) \(\Rightarrow a=n_{CO\left(p/ứ\right)}=0,16\left(mol\right)\)
\(\Rightarrow n_{Fe_3O_4}=0,04\left(mol\right)\) \(\Rightarrow m_{Fe_3O_4}=0,04\cdot232=9,28\left(g\right)\)

\(n_{Ba}=\dfrac{24,66}{137}=0,18\left(mol\right)\\
pthh:Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\)
0,18 0,18
\(\Rightarrow V_{H_2}=0,18.22,4=4,032\left(L\right)\\
n_{CuO}=\dfrac{15,2}{80}=0,19\left(mol\right)\\
pthh:H_2+CuO\underrightarrow{t^o}Cu+H_2O\)
\(LTL:0,18< 0,19\)
=> CuO dư
theo pthh : \(n_{CuO\left(p\text{ư}\right)}=n_{Cu}=n_{H_2}=0,18\left(mol\right)\)
=> \(m_{Kl}=\left(64.0,18\right)+\left(80.0,1\right)=19,52\left(g\right)\)

a) \(n_{Al}=\dfrac{10,8}{27}=0,4\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
0,4---------------------->0,6
=> V = 0,6.22,4 = 13,44 (l)
b)
\(n_{Fe_3O_4}=\dfrac{29}{232}=0,125\left(mol\right)\)
Gọi số mol Fe3O4 pư là a (mol)
PTHH: Fe3O4 + 4H2 --to--> 3Fe + 4H2O
Xét tỉ lệ: \(\dfrac{0,125}{1}< \dfrac{0,6}{4}\) => Hiệu suất tính theo Fe3O4
PTHH: Fe3O4 + 4H2 --to--> 3Fe + 4H2O
a----------------->3a
=> 232(0,125-a) + 56.3a = 22,6
=> a = 0,1
=> \(H\%=\dfrac{0,1}{0,125}.100\%=80\%\)
nAl = 10,8 : 27 = 0,4 (mol)
pthh : Al + 6HCl-t--> AlCl3 + H2
0,4--->2,4 (mol)
=> V= VO2 = 2,4 . 22,4 = 53,76 ( l)
nFe3O4 = 29 : 232 = 0,125 (mol)
pthh Fe3O4 + 4H2 -t--> 3Fe+ 4H2O
0,125----------------->0,375 (mol)
nFe (tt ) = 22,6 : 56 = 0,403 (mol )
%H = 0,375 / 0,403 . 100 % = 93 %

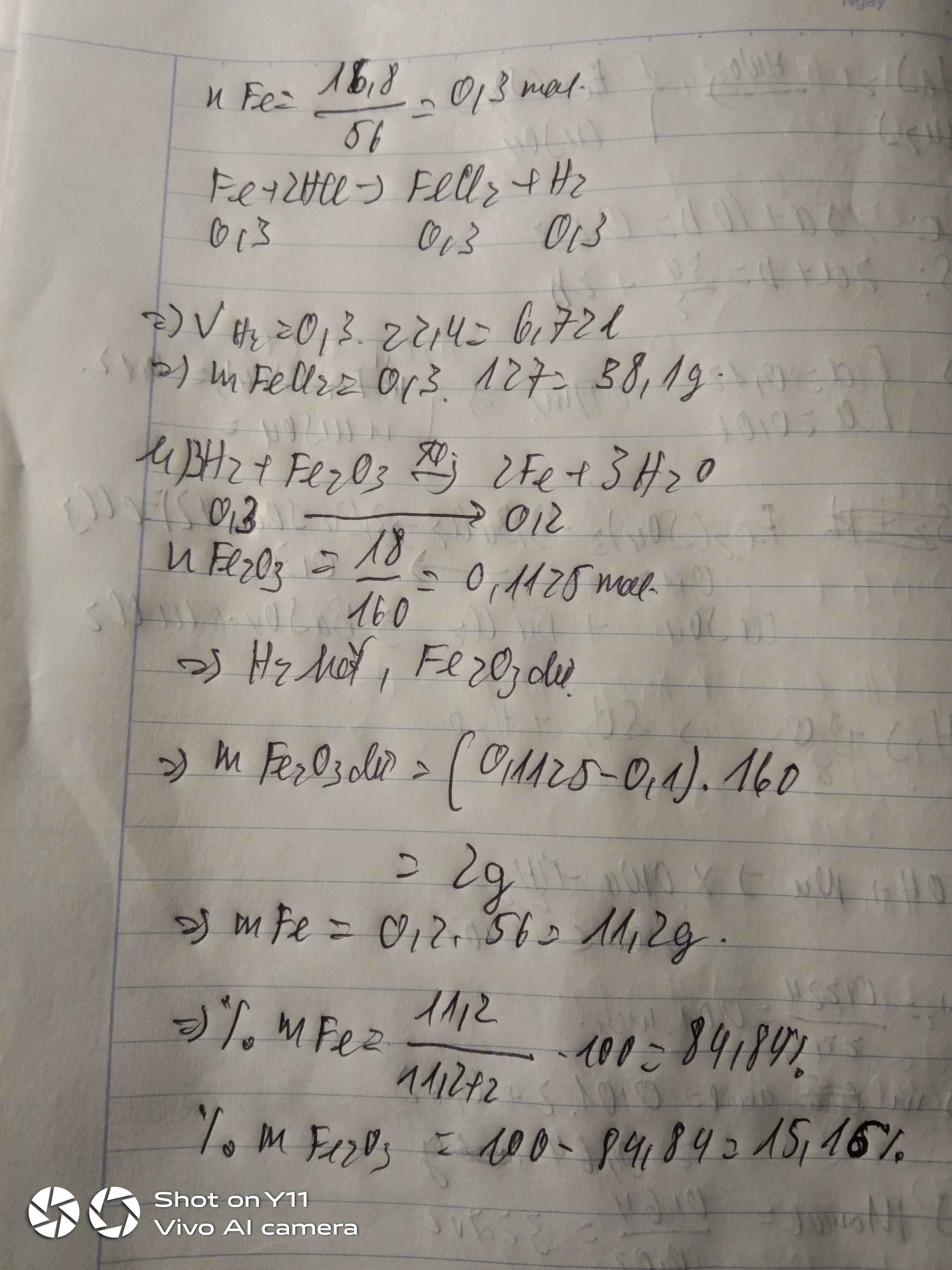
nH2 = 6,62/22,4 = 0,3 (mol)
nFe3O4 = 46,4/232 = 0,2 (mol)
PTHH: Fe3O4 + 4H2 -> (t°) 3Fe + 4H2O
LTL: 0,2 > 0,3/4 => Fe3O4 dư
nFe = 0,3 : 4 . 3 = 0,225 (mol)
mFe = 0,225 . 56 = 12,6 (g)
4H2+Fe3O4-to>3Fe+4H2O
0,3---------------------0,225 mol
n H2=\(\dfrac{6,72}{22,4}\)=0,3 mol
n Fe3O4=\(\dfrac{46,4}{232}\)=0,2 mol
=>Fe3O4 dư
=>m Fe=0,225.56=12,6g