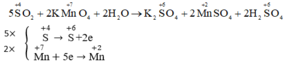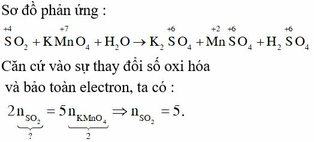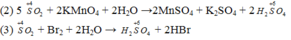Cho phản ứng: KMnO4+SO2+H2O MnSO4 + K2SO4+ H2SO4. Cho 5,6 lít khí SO2 (ở đktc) tác dụng với dung dịch KMnO4 2M. Tính thể tích dung dịch KMnO4 cần dùng cho phản ứng trên là:
A. 50ml B. 60ml C. 500ml D. 40ml
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Quan sát phương trình phản ứng ta thấy S tăng từ mức oxi hóa +4 lên mức oxi hóa +6; Mn giảm từ mức oxi hóa +7 xuống mức oxi hóa +2 → SO2 là chất khử và KMnO4 là chất oxi hóa.
5 x S + 4 → S + 6 + 2 e
2 x M n + 7 + 5 e → M n + 2
Suy ra phương trình phản ứng đã cân bằng như sau:
5SO2 + 2KMnO4 + 2H2O → K2SO4 + 2MnSO4 + 2H2SO4
Chọn đáp án A.

a)
- Quá trình oxi hóa: \(\overset{-1}{2Cl}\rightarrow\overset{0}{Cl_2}+2e\) (Nhân với 5)
- Quá trình khử: \(\overset{+7}{Mn}+5e\rightarrow\overset{+2}{Mn}\) (Nhân với 2)
PTHH: \(16HCl+2KMnO_4\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
b)
- Quá trình oxi hóa: \(\overset{+4}{S}\rightarrow\overset{+6}{S}+2e\) (Nhân với 5)
- Quá trình khử: \(\overset{+7}{Mn}+5e\rightarrow\overset{+2}{Mn}\) (Nhân với 2)
PTHH: \(5SO_2+2KMnO_4+2H_2O\rightarrow K_2SO_4+2MnSO_4+2H_2SO_4\)
c)
- Quá trình oxi hóa: \(\overset{+2}{2Fe}\rightarrow\overset{+3}{Fe_2}+2e\) (Nhân với 5)
- Quá trình khử: \(\overset{+7}{Mn}+5e\rightarrow\overset{+2}{Mn}\) (Nhân với 2)
PTHH: \(10FeSO_4+2KMnO_4+8H_2SO_4\rightarrow K_2SO_4+2MnSO_4+5Fe_2\left(SO_4\right)_3+8H_2O\)
d)
- Quá trình oxi hóa: \(\overset{+2}{2Fe}\rightarrow\overset{+3}{Fe_2}+2e\) (Nhân với 3)
- Quá trình khử: \(\overset{+6}{Cr_2}+6e\rightarrow\overset{+3}{Cr_2}\) (Nhân với 1)
PTHH: \(6FeSO_4+K_2Cr_2O_7+7H_2SO_4\rightarrow K_2SO_4+Cr_2\left(SO_4\right)_3+3Fe_2\left(SO_4\right)_3+7H_2O\)

Phương trình hóa học của phản ứng:
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
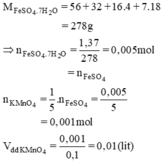

10FeSO4 + 2KMnO4 + 8H2SO4 -> 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
\(nFeSO4.7H2O=\dfrac{1.39}{56+32+64+7\times18}=5\times10^{-3}mol\) = nFeSO4
=> \(nKMnO4=5\times10^{-3}\times\dfrac{1}{5}=10^{-3}mol\)
=> VddKMnO4 = \(\dfrac{10^{-3}}{0.1}=0.01l\)

Câu đầu thiếu KCl nhé.
2FeCl3 + 2KI \(\rightarrow\) 2FeCl2 + I2 + 2KCl
Câu 2 là Cr2 nhé.
6K2S + 2K2Cr2O7 + 14H2SO4 \(\rightarrow\) 6S + 2Cr2(SO4)3 + 8K2SO4 + 14H2O
5K2SO3 + 2KMnO4 + 6KHSO4 \(\rightarrow\) 9K2SO4 + 2MnSO4 + 3H2O
5SO2 + 2KMnO4 + 2H2O \(\rightarrow\) K2SO4 + 2MnSO4 + 2H2SO4
Câu 5 S nhé.
5K2S + 2KMnO4 + 8H2SO4 \(\rightarrow\) 6K2SO4 + 2MnSO4 + 8H2O + 5S
5HCl + HClO3 \(\rightarrow\) 3Cl2 + 2H2O

- PT: a, \(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\) (1)
\(MnO_2+4HCl_đ\underrightarrow{t^o}MnCl_2+Cl_2+2H_2O\) (2)
- Ta có: \(n_{HCl\left(1\right)}=n_{HCl\left(2\right)}=0,2.2=0,4\left(mol\right)\)
Theo PT (1): \(n_{Cl_2}=\dfrac{5}{16}n_{HCl\left(1\right)}=0,125\left(mol\right)\Rightarrow V_1=0,125.22,4=2,8\left(l\right)\)
(2): \(n_{Cl_2\left(2\right)}=\dfrac{1}{4}n_{HCl\left(2\right)}=0,1\left(mol\right)\Rightarrow V_2=0,1.22,4=2,24\left(l\right)\)