Một dd A có chứa AlCl3 và FeCl3. Thêm dần dd NaOH vào 100 ml ddA cho đến dư, sau đó lọc lấy kết tủa rửa sạch sấy khô và nung ở nhiệt độ cao đến khối lượng không đổi thu được 2 gam. Mặt khác người ta phải dùng hết 40ml dung dịch AgNO3 2M mới tác dụng vừa đủ với các muối clorua có trong 50ml ddA.Tính nồng độ mol của AlCl3 có trong dung dịch A
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


trích từng mẫu thử cho tác dụng với nước :
- chất rắn không tan( hiện tượng kết tủa): BaCO3 và BaSO 4
- không có hiện tượng NaCl và Na2CO3
Sục CO2 vào 2 lọ đựng BaCO3 và BaSO 4
- kết tủa tan thì đó là lọ đựng BaCO3
- còn lọ đựng BaSO4 k có hiện tượng
BaCO3 + CO2 +H2O ----------> Ba(HCO3)2
Cho Ba(HCO3)2 vừa tạo ra vào 2 lọ muối Na
- Lọ nào k phản ứng là lọ đựng NaCl
- Lọ nào tạo ra kết tủa là Na2CO3
Na2CO3 + Ba(HCO3 )2 ----------> NaHCO3 + BaCO3

+FeCl3 tác dụng tạo thành kết tủa màu nâu đỏ Fe(OH)3.
FeCl3+3NaOH=>Fe(OH)3↓+3NaCl
0.025.....................0.025..........
+AlCl3 tác dụng tạo thành kết tủa keo trắng nhưng sau đó tan dần:
AlCl3+3NaOH=>Al(OH)3↓+3NaCl
17/600...................................
Al(OH)3+NaOH=>NaAlO2+2H2O
_Nhiệt phân Fe(OH)3 ta thu được chất rắn là Fe2O3:
+nFe2O3 = 2/160 = 0.0125(mol)
2Fe(OH)3(t*)=>Fe2O3+3H2O
0.025................0.0125.....(mol)
=>nFeCl3 = 0.025 (mol)
=>CM(FeCl3) = 0.025/0.1 = 0.25(M)
_Cho dd A tác dụng với dd AgNO3:
+nAgNO3 = 0.2*0.4 = 0.08(mol)
_Vì chỉ lấy 50ml dd A tức là kém 2 lần so với ban đầu:
=>nFeCl3(sau) = 0.025/2 = 0.0125(mol)
FeCl3+3AgNO3=>Fe(NO3)3+3AgCl↓(1)
0.0125.0.0375......(mol)
AlCl3+3AgNO3=>Al(NO3)3+3AgCl↓(2)
17/1200.0.0425....(mol)
=>nAgNO3(2) = 0.08-0.0375 = 0.0425 (mol)
=>nAlCl3(sau) = 0.0425/3 = 17/1200 (mol)
+nAlCl3(đầu) = 17/1200*2 = 17/600 (mol)
=>CM(AlCl3) = 17/600 / 0.1 ≈ 0.283(M)

\(3NaOH+FeCl_3\rightarrow Fe\left(OH\right)_3+3NaCl\)
\(n_{NaCl}=n_{NaOH}=0,2.3=0,6\left(mol\right)\)
=> \(C_{M\left(NaCl\right)}=\dfrac{0,6}{0,2}=3M\)
\(n_{Fe\left(ỌH\right)_3}=\dfrac{1}{3}n_{NaOH}=0,2\left(mol\right)\)
\(2Fe\left(OH\right)_3-^{t^o}\rightarrow Fe_2O_3+3H_2O\)
Ta có \(n_{Fe_2O_3}=\dfrac{1}{2}n_{Fe\left(OH\right)_3}=0,1\left(mol\right)\)
=> m Fe2O3 = 0,1 . 160=16(g)

Đáp án A
Nếu Mg còn dư trong phản ứng
=> mthanh hợp kim tăng = (64-24).0,075=3g > 1,16 g
=> Chứng tỏ Mg phản ứng hết.
Đặt số mol Mg và Fe phản ứng lần lượt là x, y.
=> mthanh hợp kim tăng =x(64-24)+y(64-56)=1,16g
Có ![]()
=> NaOH phản ứng với Y còn dư => 5 gam chất rắn gồm MgO, Fe2O3, có thể có CuO
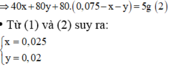
Đặt số mol Al và Fe còn dư lần lượt là a, b
=> mthanh hợp kim = 108a+24.0,025+56.(0,02+b)=8,8g
→ BTe a + 3 b + 2 . ( 0 , 025 + 0 , 02 ) = 2 . n S O 2 = 2 . 2 , 576 22 , 4 = 0 , 23 m o l


Đáp án B
Có khối lượng chất rắn sau khi nung < mX
=> Chứng tỏ X phản ứng còn dư, Cu(NO3)2 phản ứng hết.
· Trường hợp 1: Mg phản ứng còn dư.
Áp dụng tăng giảm khối lượng có:
nMg phản ứng 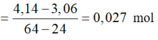
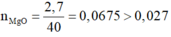 => Vô lý
=> Vô lý
· Trường hợp 2: Fe đã tham gia phản ứng.
Đặt số mol Mg và Fe phản ứng lần lượt là a, b.
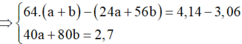
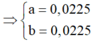
![]()
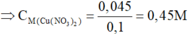

Chọn đáp án B.
Có khối lượng chất rắn sau khi nung < mX
=> Chứng tỏ X phản ứng còn dư, Cu(NO3)2 phản ứng hết.
· Trường hợp 1: Mg phản ứng còn dư.
Áp dụng tăng giảm khối lượng có:
nMg phản ứng = 4 , 14 - 3 , 06 64 - 24 = 0 , 027 mol
n M g O = 2 , 7 40 = 0 , 0675 > 0 , 027 => Vô lý
· Trường hợp 2: Fe đã tham gia phản ứng.
Đặt số mol Mg và Fe phản ứng lần lượt là a, b.
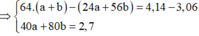
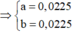
⇒ n C u N O 3 2 = 0 , 045 m o l
⇒ C M ( C u N O 3 2 ) = 0 , 045 0 , 1 = 0 , 45 M

cảm ơn bạn rất nhiều ạ