Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) \(n_{Al}=\dfrac{0,54}{27}=0,02\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
_____0,02->0,06---->0,02--->0,03
=> VH2 = 0,03.22,4 = 0,672 (l)
b) mHCl = 0,06.36,5 = 2,19 (g)
=> \(C\%_{ddHCl}=\dfrac{2,19}{100}.100\%=2,19\%\)
`a)`
`2Al+6HCl->2AlCl_3+3H_2`
`n_{Al}={0,54}/{27}=0,02(mol)`
`n_{H_2}=3/{2}n_{Al}=0,03(mol)`
`V_{H_2}=0,03.22,4=0,672(l)`
`b)`
`n_{HCl}=2n_{H_2}=0,06(mol)`
`C%_{HCl}={0,06.36,5}/{100}.100%=2,19%`

a, PT: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
b, Ta có: \(n_{Fe}=\dfrac{19,6}{56}=0,35\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Fe}=0,35\left(mol\right)\Rightarrow V_{H_2}=0,35.22,4=7,84\left(l\right)\)
c, \(n_{H_2SO_4}=n_{Fe}=0,35\left(mol\right)\Rightarrow C_{M_{H_2SO_4}}=\dfrac{0,35}{0,2}=1,75\left(M\right)\)
d, \(n_{FeSO_4}=n_{Fe}=0,35\left(mol\right)\Rightarrow m_{FeSO_4}=0,35.152=53,2\left(g\right)\)
e, \(C_{M_{FeSO_4}}=\dfrac{0,35}{0,2}=1,75\left(M\right)\)
d, \(n_{H_2SO_4}=0,25.1,6=0,4\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{n_{Fe}}{1}< \dfrac{n_{H_2SO_4}}{1}\), ta được H2SO4 dư.
Theo PT: \(n_{H_2SO_4\left(pư\right)}=n_{Fe}=0,35\left(mol\right)\)
\(\Rightarrow n_{H_2SO_4\left(dư\right)}=0,4-0,35=0,05\left(mol\right)\)
\(\Rightarrow m_{H_2SO_4\left(dư\right)}=0,05.98=4,9\left(g\right)\)

Ta có: \(n_{Mg}=\dfrac{14,4}{24}=0,6\left(mol\right)\)
a, PT: \(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
_____0,6____________________0,6 (mol)
\(\Rightarrow V_{H_2}=0,6.22,4=13,44\left(l\right)\)
b, Ta có: \(n_{Fe_2O_3}=\dfrac{32}{160}=0,2\left(mol\right)\)
PT: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
Xét tỉ lệ: \(\dfrac{0,2}{1}=\dfrac{0,6}{3}\), ta được pư hết.
Theo PT: \(n_{Fe}=2n_{Fe_2O_3}=0,4\left(mol\right)\)
\(\Rightarrow m_{Fe}=0,4.56=22,4\left(g\right)\)
Bạn tham khảo nhé!

\(n_{Fe}=\dfrac{22,4}{56}=0,4\) (mol) (1)
Phương trình hóa học :
Fe + 2HCl ---> FeCl2 + H2 (2)
Từ (1) và (2) ta có \(n_{FeCl_2}=n_{H_2}=0,4\) (mol) ; \(n_{HCl}=0,8\left(mol\right)\)
b) => \(m_{\text{muối}}=0,4.\left(56+35,5.2\right)=50.8\left(g\right)\)
c) \(V_{\text{khí}}=0,4.22,4=8,96\left(l\right)\)
d) \(m_{HCl}=0,8.36.5=29,2\left(g\right)\)
\(\Rightarrow C\%=\dfrac{29,2}{200}.100\%=14,6\%\)

nFe=0,1 mol
Fe +2HCl=>FeCl2+H2
0,1 mol=>0,2 mol =>0,1 mol
VH2=0,1.22,4=2,24 lít
nHCl=0,2 mol=>mHCl=0,2.36,5=7,3g
=>C% dd HCl=7,3/200.100%=3,65%
a ,\(Zn+2HCl=>ZnCl_2+H_2\) (1)
b, \(n_{Zn}=\frac{6,5}{65}=0,1\left(mol\right)\)
theo (1) \(n_{H_2}=n_{Zn}=0,1\left(mol\right)\)
=> \(V_{H_2}=0,1.22,4=2,24\left(l\right)\)
c, Theo (1) \(n_{HCl}=2n_{Zn}=0,2\left(mol\right)\)
=> \(m_{HCl}=0,2.36,5=7,3 \left(g\right)\)
nồng độ % dung dịch axit đã dùng là
\(\frac{7,3}{200}.100\%=36,5\%\)

\(n_{Mg}=\dfrac{12}{24}=0,5\left(mol\right)\)
PT: \(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
a, \(n_{H_2}=n_{Mg}=0,5\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,5.22,4=11,2\left(l\right)\)
b, \(n_{H_2SO_4}=n_{Mg}=0,5\left(mol\right)\)\(\Rightarrow C_{M_{H_2SO_4}}=\dfrac{0,5}{0,2}=2,5\left(M\right)\)

số mol kẽm phản ứng: \(n_{Zn}=\frac{m}{M}=\frac{6,5}{65}=0,1\left(mol\right)\)
PTHH:
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
0,1 0,1 0,1 (mol)
a,Thể tích khí H2 thu được là:\(V_{H_2}=n_{H_2}\times22,4=0,1\times22,4=2,24\left(l\right)\)
b,Thể tích dung dịch H2SO4 1M đã dùng:
\(V_{H_2SO_4}=\frac{n_{H_2SO_4}}{C_M}=\frac{0,1}{1}=0,1\left(l\right)=100\left(ml\right)\)

a.
n Fe=28562856=0,5 (mol)
Fe+H2SO4→FeSO4+H2↑
0,5→0,5 0,5 0,5 (mol)
b.
V H2(đktc)=0,5.22,4=11,2 (l)
c.
m HCl=0,5.36,5=18,25 (g)
d.
m FeSO4=0,5.152=76 (g)
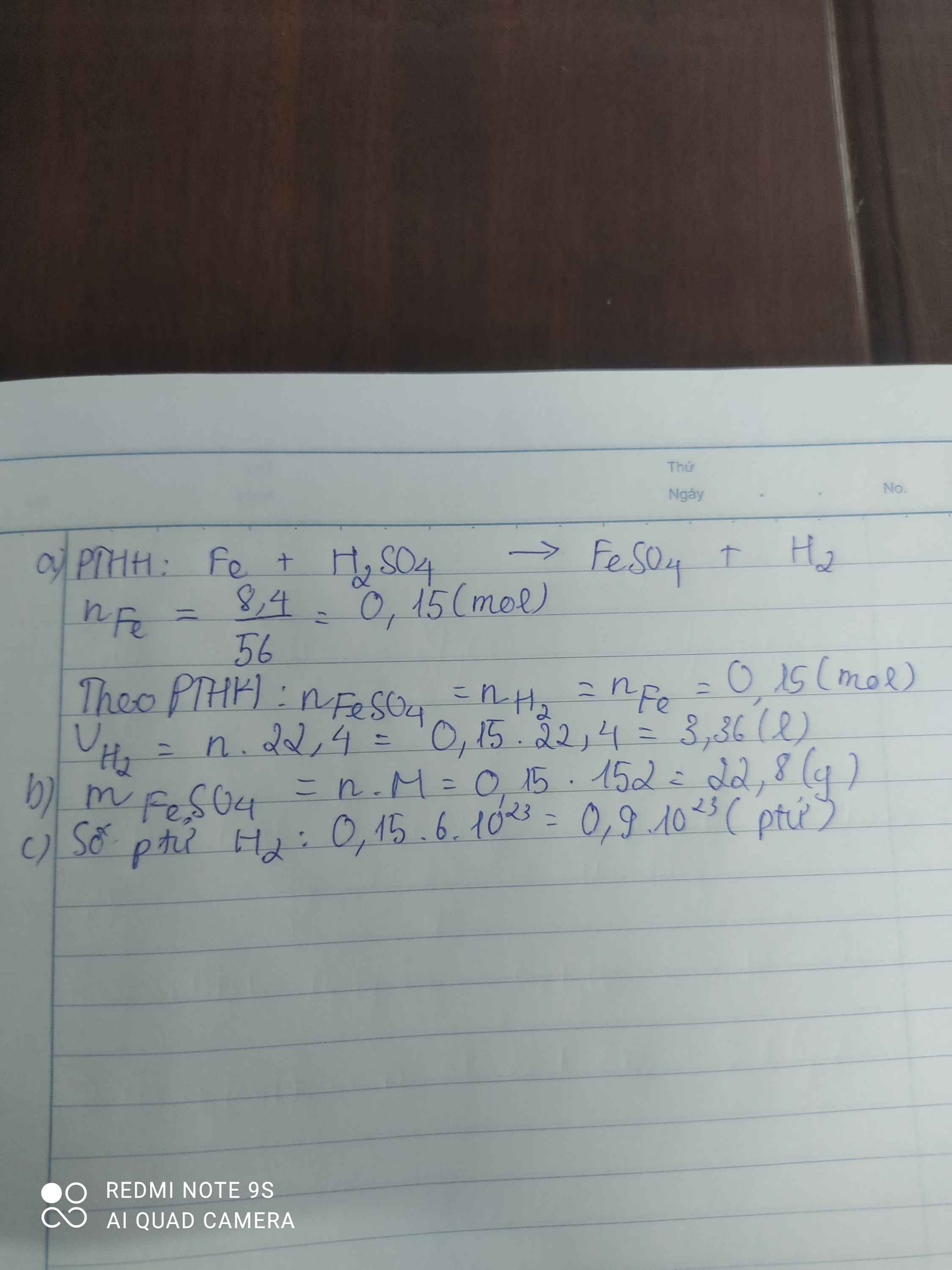
hình như sai đề