Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

n CO2 =0,07 MOL
n NaOH = 6,4:(23+16+1)=0,16 mol
t = n NaOH / CO2 = 0,16/0,7 16/7 > 2
=> muối tạo thành là Na2CO3
\(2NaOH+CO_2->Na_2CO_3+H_2O\)
Bđ 0,16............0,07
Pư 0,14............0,07........0,07
spu 0,02............0............0,07
m Na2CO3 = 0,07.(23.2+12+16.3)=7,42 g

Chọn B
Khối lượng muối thu được: Trước tiên ta phải xem muối nào được tạo thành (NaHC O 3 hay N a 2 C O 3 )
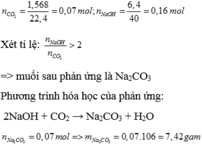

\(n_{SO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right);n_{NaOH}=\dfrac{140.20\%}{40}=0,7\left(mol\right)\\ Vì:\dfrac{n_{NaOH}}{n_{SO_2}}=\dfrac{0,7}{0,3}>2\Rightarrow SP:Na_2SO_3.Có:NaOH\left(dư\right)\\ PTHH:2NaOH+SO_2\rightarrow Na_2SO_3+H_2O\\ n_{NaOH\left(dư\right)}=0,7-0,3.2=0,1\left(mol\right)\\ m_{NaOH\left(dư\right)}=0,1.40=4\left(g\right)\\ n_{Na_2SO_3}=n_{SO_2}=0,3\left(mol\right)\\ m_{Na_2SO_3}=126.0,3=37,8\left(g\right)\)

\(n_{CO_2}=\dfrac{1,568}{22,4}=0,07\left(mol\right)\\ n_{NaOH}=\dfrac{6,4}{40}=0,16\left(mol\right)\)
\(T=\dfrac{n_{NaOH}}{n_{CO_2}}=\dfrac{0,16}{0,7}\approx2,2\rightarrow\) Tạo muối trung hoà
PTHH: 2NaOH + CO2 ---> Na2CO3 + H2O
LTL: \(\dfrac{0,16}{2}>0,07\rightarrow\) NaOH dư
Theo pthh: \(\left\{{}\begin{matrix}n_{NaOH\left(pư\right)}=2n_{CO_2}=0,07.2=0,14\left(mol\right)\\n_{Na_2CO_3}=n_{CO_2}=0,07\left(mol\right)\end{matrix}\right.\)
\(\rightarrow m_{sau.pư}=\left(0,16-0,14\right).40+0,07.106=8,22\left(g\right)\)

\(n_{CO_2}=\dfrac{1,568}{22,4}=0,07\left(mol\right);n_{NaOH}=\dfrac{6,4}{40}=0,16\left(mol\right)\)
PTHH: CO2 + 2NaOH → Na2CO3 + H2O
Mol: 0,07 0,14 0,07
Ta có: \(\dfrac{0,07}{1}< \dfrac{0,16}{2}\) ⇒ CO2 hết, NaOH dư
\(m_{Na_2CO_3}=0,07.106=7,42\left(g\right)\)
\(m_{NaOHdư}=\left(0,16-0,14\right).40=0,8\left(g\right)\)

Đáp án D
nCO2 = 1,568: 22,4 = 0,07 mol ; nNaOH = 3,2: 40 = 0,08 mol
=> Ta thấy: nCO2 < nNaOH < 2nCO2 => tạo cả 2 muối CO32- và HCO3-
=> nNa2CO3 = nNaOH – nCO2 = 0,08 – 0,07 = 0,01 mol
Và nNaHCO3 = nCO2 – nNa2CO3 = 0,07 – 0,01 = 0,06 mol
=> mmuối = mNa2CO3 + mNaHCO3 = 106.0,01 + 84.0,06 = 6,1g

Số mol: nCO2 = 1,56822,41,56822,4 = 0,07 mol; nNaOH = 6,4406,440 = 0,16 mol
Phương trình hóa học:
2NaOH + CO2 → Na2CO3 + H2O
Lúc ban đầu: 0,07 0,16 0 (mol)
Phản ứng: 0,07 → 0,14 0,07
Sau phản ứng: 0 0,02 0,07
a)Chất còn dư là NaOH và dư: 0,02×40 = 0,8 g
b)Khối lượng muối Na2CO3 tạo thành là: 0,07×106 = 7,42 g.
*TK
$n_{CO_2} = \dfrac{1,568}{22,4} = 0,07(mol) ; n_{NaOH} = \dfrac{6,4}{40} = 0,16(mol)$
$n_{NaOH} : n_{CO_2} = 0,16 : 0,07 = 2,2 > 2$. Do đó, NaOH dư
$2NaOH +C O_2 \to Na_2CO_3 + H_2O$
$n_{Na_2CO_3} = n_{CO_2} = 0,07(mol)$
$m_{Na_2CO_3} = 0,07.106 = 7,42(gam)$
$n_{NaOH\ pư} = 2n_{CO_2} = 0,14(mol)$
$m_{NaOH\ dư} = 6,4 - 0,14.40 = 0,8(gam)$
a, Ta có: \(n_{CO_2}=\dfrac{1,568}{22,4}=0,07\left(mol\right)\)
\(n_{NaOH}=\dfrac{6,4}{40}=0,16\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{n_{NaOH}}{n_{CO_2}}=\dfrac{0,16}{0,07}=2,29>2\)
Vậy: Pư tạo muối Na2CO3 và NaOH dư.
b, PT: \(CO_2+2NaOH\rightarrow Na_2CO_3+H_2O\)
Theo PT: \(n_{Na_2CO_3}=n_{CO_2}=0,07\left(mol\right)\)
\(\Rightarrow m_{Na_2CO_3}=0,07.106=7,42\left(g\right)\)
Bạn tham khảo nhé!