Điện phân dung dịch KCl bão hòa, có màng ngăn giữa hai điện cực. Sau một thời gian điện phân, dung dịch thu được có môi trường
A. axit yếu
B. trung tính
C. axit mạnh
D. kiềm.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn C.
Dung dịch Y có chứa OH- Þ
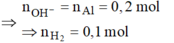
Khí thoát ra ở cả 2 điện cực là H2 và Cl2 với M = 57,2 Þ n Cl 2 = 0 , 4 mol
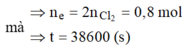

Chọn C.
Dung dịch Y có chứa OH-
![]()
Khí thoát ra ở cả 2 điện cực là H2 và Cl2 với M = 57,2
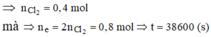

Chọn đáp án D
nKhí ở anot = 0,14 > 0,24/2 Þ Có tạo O2 với nO2 = 0,14 – 0,24/2 = 0,02
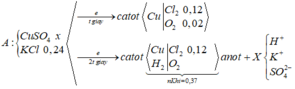
Tại t giây có ne = 0,12 x 2 + 0,02 x 4 = 0,32 Þ Tại 2t giây có ne = 0,32 x 2 = 0,64
Þ nO2 tại 2t giây = (0,64 - 0,12 x 2)/4 = 0,1 Þ nH2 = 0,37 - 0,12 - 0,1 = 0,15
Þ nCu tại 2t giây = 0,64/2 - 0,15 = 0,17 Þ x = 0,17 Þ nSO42- trong X = 0,17
BTNT.K Þ nK+ = 0,24; BTĐT trong X Þ nH+ = 0,17 x 2 - 0,24 = 0,1 Þ [H+] = 0,1M Þ pH = y = 1

Đáp án D
Thời gian điện phân t:
n k h í = 3 , 136 22 , 4 = 0,14 mol
Anot:
Cl- → Cl2 +2e
0,24 0,12 0,24 mol
H2O → H+ + O2 + 4e
0,02 0,08 mol
ne trao đổi = 0,32 mol
ne trao đổi = I t F
=> thời gian 2t, ne trao đổi = 0,64 mol
thời gian điện phân 2t nkhí = 0,37 mol
khi đó anot :
Cl- → Cl2 + 2e
0,24 0,12 0,24 mol
H2O → H+ + O2 + 4e
0,1 0,4 mol
=> n H 2 = 0,37- 0,12 – 0,1 = 0,15 mol
catot:
Cu2+ +2e → Cu
x 2x x mol
H2O + 2e → 2OH- + H2
0,15 0,3 0,3 0,15 mol
2x+0,3 = 0,64
=> x = 0,17 mol
mặt khác
nH+ =0,1 mol ⇒ [H+] = 0,1
⇒ pH = 1
Đáp án D