Cho 400 ml dung dịch Ba(OH)2 0,5M vào 100 ml dung dịch Al2(SO4)3 0,5M, thu được m gam kết tủa. Giá trị của m là
A. 37,29.
B. 34,95.
C. 46,60.
D. 36,51.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Số mol Fe = 0,02 mol; số mol Cu = 0,03 mol; số mol H+ = 0,4 mol;
số mol NO3- = 0,08 mol
Các phản ứng xảy ra:
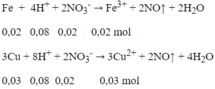
Sau 2 phản ứng trên, trong dung dịch X có 0,02 mol Fe3+; 0,03 mol Cu2+ và 0,24 mol H+ dư, ngoài ra còn có ion NO3- và SO42-. Tuy nhiên chỉ có 3 loai ion đầu là phản ứng với OH-.
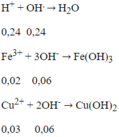
Tổng số mol OH- = 0,24 + 0,06 + 0,06 = 0,36 mol
→ V = 360ml

Đáp án B
n C O 2 = 0 , 2 m o l
Cho 100 ml dung dịch X vào dung dịch chứa 0,15 mol HCl thu được 0,12 mol CO2.
Do n C O 2 < n H C l < 2 n C O 2 nên dung dịch X chứa K2CO3 và KHCO3.
Gọi số mol K2CO3 và KHCO3 phản ứng lần lượt là a, b.
=> a+b= 0,12; 2a+b=0,15
Giải được a=0,03; b=0,09 vậy trong X tỉ lệ số mol K2CO3 và KHCO3 là 1:3.
Gọi số mol K2CO3 trong X là m suy ra KHCO3 là 3m.
Cho 100 ml dung dịch X tác dụng với Ba(OH)2 dư thu được 0,2 mol kết tủa BaCO3.
Do vậy 200 ml dung dịch X tác dụng thì thu được 0,4 mol kết tủa.
=> m+3m= 0,4=> m=0,1
Bảo toàn C: n K 2 C O 3 = 0 , 4 - 0 , 2 = 0 , 2
Bảo toàn K: n K O H = 0 , 1 . 2 + 0 , 3 - 0 , 2 . 2 = 0 , 1
Vậy x= 0,1

Đáp án B
n C O 2 = 0 , 2 m o l
Cho 100 ml dung dịch X vào dung dịch chứa 0,15 mol HCl thu được 0,12 mol CO2.
Do n C O 2 < n H C l < 2 n C O 2 nên dung dịch X chứa K2CO3 và KHCO3.
Gọi số mol K2CO3 và KHCO3 phản ứng lần lượt là a, b.
=> a + b = 0,12; 2a + b = 0,15
Giải được a=0,03; b=0,09 vậy trong X tỉ lệ số mol K2CO3 và KHCO3 là 1:3.
Gọi số mol K2CO3 trong X là m suy ra KHCO3 là 3m.
Cho 100 ml dung dịch X tác dụng với Ba(OH)2 dư thu được 0,2 mol kết tủa BaCO3.
Do vậy 200 ml dung dịch X tác dụng thì thu được 0,4 mol kết tủa.
=> m + 3m = 0,4 => m = 0,1
Bảo toàn C: n K 2 C O 3 = 0,4 - 0,2 = 0,2 mol
Bảo toàn K: n K O H = 0,1.2 + 0,3 - 0,2.2 = 0,1
Vậy x=0,1

Đáp án : B
,nCO2 bđ = 0,4 mol
100 ml X + Ba(OH)2 -> nBaCO3 = nC(X) = 0,2 mol
=> Trong 400 ml X có 0,8 mol C => Bảo toàn C : nCO2 bđ + nK2CO3 = nC(X)
=> nK2CO3 = y = 0,4 mol
Giả sử trong 200 ml X có a mol K2CO3 và b mol KHCO3 ( a + b = 0,4 mol)
Cho từ từ X vào nHCl = 0,3 mol tạo nCO2 = 0,24 mol
=> K2CO3 và KHCO3 phản ứng đồng thời (vì HCl lúc đầu dư) theo tỉ lệ mol a : b
Gọi nK2CO3 pứ = ax và nKHCO3 pứ = bx
=> 2ax + bx = nHCl = 0,3 mol ; ax + bx = nCO2 = 0,24 mol
=> ax = 0,06 và bx = 0,18 mol
=> a : b = 1 : 3
=> a = 0,1 ; b = 0,3 mol
=> Bảo toàn K : x + 2y = 2.(2a + b)
=> x = 0,2 mol

Đáp án C
Pt pư:
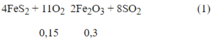
Ta có: nBaC03 = 0,15 mol
nKOH = 0,1 mol ⇒ nBa2+ = 0,15 mol ; nOH- = 0,4 mol
Khi cho SO2 vào dung dịch Y thu được 21,7 (g) BaSO3. Cho Y tác dụng với dung dịch NaOH thấy xuất hiện thêm kết tủa, chứng tỏ trong dung dịch Y có ion HSO3-.
Vì: Ba2+ + HSO3- + OH- " BaSO3 + H2O
Ta có: nBaC03 = 0,1 mol
Ptpứ:
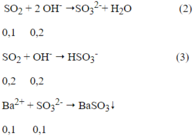
Ta có: nOH- = 0,4 - 0,2 = 0,2 mol
Theo ptpư (2), (3) ta có: n SO2= 0,1 + 0,2 = 0,3 mol
Theo ptpư (1) ta có: n FeS2 = ½ n SO2= 0,15 mol ⇒ m FeS2 = 120.0,15 = 18(g)
Đáp án B