Câu 1: Cho các chất sau: Cu ; SO2; PbO ; HgO ; O2 , Na, BaO, CuO, K , MgO
a) Chất nào tác dụng được với H? Viết phương trình
b) Chất nào tác dụng với H2O? Viết phương trình
Câu 2: Nêu hiện tượng trong thí nghiệm sau:
a) Dẫn H dư qua ống nghiệm đựng CuO đun nóng
b) Thả 1 mẩu kém vào dung dịch HCl
c) Thả 1 mẩu Natri vào nước rồi đun quỳ tím vào dung dịch.
Câu 4: Hoàn thành PT sau:
a) Na + H2O ------->
b) Fe + HCl...
Đọc tiếp
Câu 1: Cho các chất sau: Cu ; SO2; PbO ; HgO ; O2 , Na, BaO, CuO, K , MgO
a) Chất nào tác dụng được với H? Viết phương trình
b) Chất nào tác dụng với H2O? Viết phương trình
Câu 2: Nêu hiện tượng trong thí nghiệm sau:
a) Dẫn H dư qua ống nghiệm đựng CuO đun nóng
b) Thả 1 mẩu kém vào dung dịch HCl
c) Thả 1 mẩu Natri vào nước rồi đun quỳ tím vào dung dịch.
Câu 4: Hoàn thành PT sau:
a) Na + H2O ------->
b) Fe + HCl -------->
c) Na2O +H2O -------->
Câu 5: Cho 5,4g Al tác dụng hoàn toàn với HCl
a) Viết phương rình? Gọi tên sản phẩm
b) Tính VH thu được ở đktc ? Và khối lượng muối tạo thành.
Các bạn giúp tớ với. Tớ cảm ơn nhiều





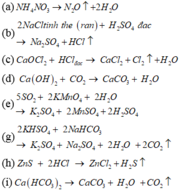
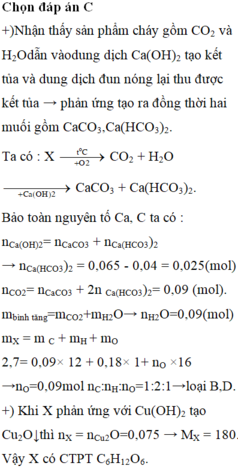

Chọn đáp án C
- C H 2 - C H O O C C H 3 - - n + H 2 O → H C l n C H 3 C O O H + - C H 2 - C H O H - n -