Cho 18,64 gam hỗn hợp gồm Na và Al2O vào lượng nước dư, thu được a mol khí H2; đồng thời còn lại 6,8 gam rắn không tan. Giá trị của a là
A. 0,16
B. 0,06
C. 0,08
D. 0,04
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

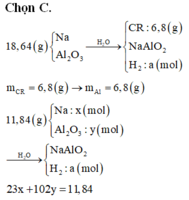
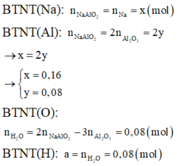

Đáp án D
6,8 chất rắn không tan là Al2O3.
m(hh phản ứng) = 18,64 – 6,8 = 11,84 gam
Na + H2O → NaOH + ½ H2
x x ½ x
2NaOH + Al2O3 → 2NaAlO2 + 2H2O
x ½ x
Nên có: 23x + 102. ½ x = 11,84 => x = 0,16 mol
→ a = ½ x = 0,08 mol

Đáp án D
6,8 chất rắn không tan là Al2O3.
m(hh phản ứng) = 18,64 – 6,8 = 11,84 gam
Na + H2O → NaOH + ½ H2
x x ½ x
2NaOH + Al2O3 → 2NaAlO2 + 2H2O
x ½ x
Nên có: 23x + 102. ½ x = 11,84
=> x = 0,16 mol
→ a = ½ x = 0,08 mol

* T N 1 : A l : a m o l N a : b m o l → H 2 O N a A l O 2 : b m o l H 2 A l B T e : n N a + 3 . n P b = b + 3 b = 2 . n H 2 = 0 , 48 → b = 0 , 12 * T N 2 : A l : 0 , 12 m o l N a : a m o l → H 2 O N a A l O 2 : 0 , 12 m o l N a O H : 0 , 03 m o l + . . . a = n N a = n N a O H + n N a A l O 2 = 0 , 15 → n A l ( T N 1 , T N 2 ) = 0 , 27 m o l → m A l = 7 , 29 g

Đáp án B
nBa2+ = n kết tủa max = 27,58/197 = 0,14 mol (tại thời điểm nCO2 = a = 0,14)
Khi nCO2 = 0,4 mol dung dịch thu được gồm: Ba2+ (0,14 mol), HCO3- (0,4 mol) và Na+
BTĐT => nNa+ = 0,12 mol
BT e: 2nBa + nNa = 2nO + 2nH2 => nO = 0,06 mol
m = mBa + mNa + mO = 22,9 gam

Đáp án B
nBa2+ = n kết tủa max = 27,58/197 = 0,14 mol (tại thời điểm nCO2 = a = 0,14)
Khi nCO2 = 0,4 mol dung dịch thu được gồm:
Ba2+ (0,14 mol), HCO3- (0,4 mol) và Na+
BTĐT => nNa+ = 0,12 mol
BT e: 2nBa + nNa = 2nO + 2nH2
=> nO = 0,06 mol
m = mBa + mNa + mO = 22,9 gam

Tại vị trí kết tủa max ta có: nBaCO3=nBa(OH)2=a=0,12mol
Tại vị trí kết tủa min ta có
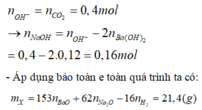
Đáp án A