Hãy chọn đáp án đúng?
Trong một cốc nước có chứa 0,01mol Na+, 0,02mol Ca2+, 0,01mol Mg2+, 0,05mol HCO3-, 0,02 mol Cl-, nước trong cốc là:
A. Nước mềm
B. Nước cứng tạm thời
C. Nước cứng vĩnh cữu
D. Nước cứng toàn phần
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C.
Cốc nước trên chứa các ion: Ca2+, Mg2+, HCO3-, Cl-
⇒ Thuộc nước cứng toàn phần (có cả tính cứng tạm thời và tính cứng vĩnh cửu)

Khi đun sôi : 2HCO3- → CO32- + CO2 + H2O
=> n CO32- = 0,025 mol tạo kết tủa với Mg2+ và Ca2+ nhưng ion kim loại này vẫn còn dư => nước trong cốc trở thành nước cứng vĩnh cửu
=>A

Giải thích:
BTĐT : │∑ n. đơn vị điện tích (+)│ = │∑ n. đơn vị điện tích (-)│
=> 0,02.1 + 0,02.2 + 0,04.2 = 0,02.1+ x
=> x = 0,16 (mol)
Để làm mềm nước cứng tức phải kết tủa hết ion Mg2+ và Ca2+→MgCO3 và CaCO3
HCO3- + OH - →CO3 2- + H2O
0,12→ 0,12
=> nOH - = 0,12 (mol) => nCa(OH)2 = 1/2 nOH- = 0,06 (mol)
=> VCa(OH)2 = n : CM = 0,06 : 0,02 = 3(M)
Đáp án D

Đáp án B
![]() có thể làm mềm nước cứng do tạo tủa trực tiếp
có thể làm mềm nước cứng do tạo tủa trực tiếp
Với ![]()
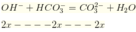
Để làm mềm nước thì kết tủa hoàn toàn ![]()
![]()
![]()
![]()
nên không thể làm mềm nước bằng C a ( O H ) 2

Đáp án C
Giải:
nMg2+ + nCa2+ = 2nHCO3- => Đun sôi cốc nước đến khi phản ứng xảy ra hoàn toàn thu ion Mg2+ và Ca2+ bị kết tủa hết

Giải thích:
Ta thấy cốc nước có chứa các ion Ca2+, Mg2+, HCO3-, Cl- => đây thuộc nước cứng toàn phần
Đáp án B
Đáp án : D