cho 200 gam dung dịch H2 SO4 9,8 % vào đd bacl2. khối lượng kết tủa thu được là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(m_{ct}=\dfrac{19,6.200}{100}=39,2\left(g\right)\)
\(n_{H2SO4}=\dfrac{39,2}{98}=0,4\left(mol\right)\)
\(m_{ct}=\dfrac{5,2.200}{100}=10,4\left(g\right)\)
\(n_{BaCl2}=\dfrac{10,4}{208}=0,05\left(mol\right)\)
Pt : \(H_2SO_4+BaCl_2\rightarrow2HCl+BaSO_4|\)
1 1 2 1
0,4 0,05 0,1 0,05
a) Lập tỉ số so sánh: \(\dfrac{0,4}{1}>\dfrac{0,05}{1}\)
⇒ H2SO4 dư , BaCl2 phản ứng hết
⇒ Tính toán dựa vào số mol của BaCl2
\(n_{BaSO4}=\dfrac{0,05.1}{1}=0,05\left(mol\right)\)
⇒ \(m_{BaSO4}=0,05.233=11,65\left(g\right)\)
b) \(n_{HCl}=\dfrac{0,05.2}{1}=0,1\left(mol\right)\)
⇒ \(m_{HCl}=0,1.36,5=3,65\left(g\right)\)
\(n_{H2SO4\left(dư\right)}=0,4-0,05=0,35\left(mol\right)\)
⇒ \(m_{H2SO4\left(dư\right)}=0,35.98=34,3\left(g\right)\)
\(m_{ddspu}=200+200-11,65=388,35\left(g\right)\)
\(C_{ddHCl}=\dfrac{3,65.100}{388,35}=0,94\)0/0
\(C_{ddH2SO4\left(dư\right)}=\dfrac{34,3.100}{388,35}=8,83\)0/0
Chúc bạn học tốt
\(a.n_{H_2SO_4}=\dfrac{200.19,6\%}{98}=0,4\left(mol\right)\\ n_{BaCl_2}=\dfrac{200.5,2\%}{208}=0,05\left(mol\right)\\ BaCl_2+H_2SO_4\rightarrow BaSO_4\downarrow+2HCl\\ Vì:\dfrac{0,05}{1}< \dfrac{0,4}{1}\\ \Rightarrow H_2SO_4dư\\ n_{BaSO_4}=n_{BaCl_2}=0,05\left(mol\right)\\ \Rightarrow m_{\downarrow}=m_{BaSO_4}=0,05.233=11,65\left(g\right)\\ b.m_{ddsau}=200+200-11,65=388,35\left(g\right)\\ C\%_{ddHCl}=\dfrac{0,05.2.36,5}{388,35}.100\approx0,94\%\\ C\%_{ddH_2SO_4\left(dư\right)}=\dfrac{\left(0,4-0,05\right).98}{388,35}.100\approx8,832\%\)

a)
$BaCl_2 + H_2SO_4 \to BaSO_4 + 2HCl$
$n_{BaCl_2} = 0,1 < n_{H_2SO_4} = 0,2$ nên $H_2SO_4$ dư
$n_{BaSO_4} = n_{BaCl_2} = 0,1(mol)$
$m_{BaSO_4} = 0,1.233 = 23,3(gam)$
b)
A gồm :
$HCl : 0,1.2 = 0,2(mol)$
$H_2SO_4\ dư : 0,2 - 0,1 = 0,1(mol)$
$V_{dd} = 0,1 + 0,1= 0,2(lít)$
$C_{M_{HCl}} = \dfrac{0,2}{0,2} = 1M$
$C_{M_{H_2SO_4}} = \dfrac{0,1}{0,2} = 0,5M$
c)
$2NaOH + H_2SO_4 \to Na_2SO_4 + 2H_2O$
$n_{NaOH} = 2n_{H_2SO_4\ dư} = 0,2(mol)$
$m_{dd\ NaOH} = \dfrac{0,2.40}{15\%} = 53,33(gam)$

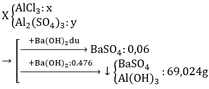
Cho Ba(OH)2 vào muối Al sẽ có 2TH sau:
TH1: kết tủa Al(OH)3 chưa bị hòa tan
Al3+ + 3OH– → Al(OH)3↓
→ nAl(OH)3 = nAl3+ → nAl(OH)3 = xn + 0,04n
TH2: kết tủa Al(OH)3 bị hòa tan một phần
Al3+ + 3OH– → Al(OH)3↓
(xn + 0,04n)→ 3(xn + 0,04n) (xn + 0,04n)
Al(OH)3 + OH– → AlO2– + 2H2O
0,952 – 3(xn + 0,04n) ←0,952
→ nAl(OH)3 = 4xn + 0,16n – 0,952


Khối lượng dd NaOH : 1,28*250= 80g => nNaOH = (80*25/100)/40 = 2mol
PT : BaCl2 + H2SO4 ----> BaSO4 + 2HCl
0,05mol --> 0,05mol
H2SO4 + 2NaOH -------> Na2SO4 + 2H2O
1mol <--- 2mol
hoep t trên ta có tổng số mol của H2SO4 : 0,05+1 = 1,05mol => mH2SO4 = 98*1,05 =102,9g
Vậy c%H2SO4 : 102,9/200*100= 51,45%

Đáp án A
• 0,3V mol NaOH + 0,04 mol Al2(SO4)3 → ↓ Al(OH)3
Nung ↓ → 0,01 mol Al2O3
→ nAl(OH)3 = 0,02 mol.
• TH1: NaOH hết
6NaOH + Al2(SO4)3 → 2Al(OH)3↓ + 3Na2SO4
nNaOH = 0,02 × 3 = 0,06 mol
→ VNaOH = 0,06 : 0,3 = 0,2 lít.
• TH2: NaOH dư
6NaOH + Al2(SO4)3 → 2Al(OH)3↓ + 3Na2SO4 (*)
NaOH + Al(OH)3 → NaAlO2 + 2H2O (**)
Theo (*) nNaOH = 0,04 × 6 = 0,24 mol; nAl(OH)3 = 0,04 × 2 = 0,08 mol.
Theo (**) nAl(OH)3 phản ứng = 0,08 - 0,02 = 0,06 mol
→ nNaOH = 0,06 mol
→ ∑nNaOH = 0,24 + 0,06 = 0,3 mol
→ VNaOH = 0,3 : 0,3 = 1 lít
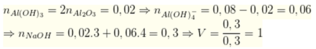

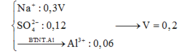
bacl2+h2so4--->baso4+2hcl
n h2so4=0,3
x=31,2%
Ta có: \(C_{\%_{H_2SO_4}}=\dfrac{m_{H_2SO_4}}{200}.100\%=9,8\%\)
\(\Rightarrow m_{H_2SO_4}=19,6\left(g\right)\)
\(\Rightarrow n_{H_2SO_4}=\dfrac{19,6}{98}=0,2\left(mol\right)\)
\(PTHH:H_2SO_4+BaCl_2--->BaSO_4\downarrow+2HCl\)
Theo PT: \(n_{BaSO_4}=n_{H_2SO_4}=0,2\left(mol\right)\)
\(\Rightarrow m_{BaSO_4}=0,2.233=46,6\left(g\right)\)