Cho 0,35 mol hỗn hợp gồm K, Ba, Na và CaO vào nước thu được 4 mol khí H2 và dung dịch Y. Hấp thụ từ từ CO2 vào dung dịch Y thì lượng kết tủa tối đa có thể thu được là 0,15 mol. Lọc kết tủa trên đem cân thì thấy khối lượng của kết tủa là 24,7 gam. Nếu cho a mol AlCl3 vào dung dịch Y thì khối lượng kết tủa thu được là
A. 4,05 gam
B. 4,50 gam
C. 5,40 gam
D. 6,75 gam


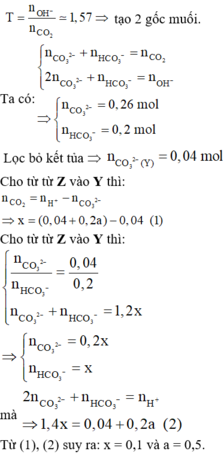



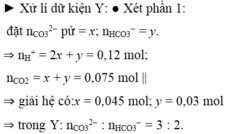





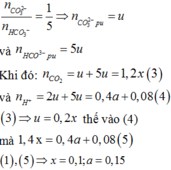
Chọn đáp án B.
nK + nNa = 0,35 – 0,15 = 0,2 => nH2 = 0,2/2 + 0,1 = 0,2 = a => nAlCl3 dùng = 0,2
=> nAl3+ = 0,2 mà nOH- = 0,2 + 0,15×2 = 0,5 < 0,1×3 => Al(OH)3 chưa đạt kết tủa tối đa
nAl(OH)3 = 0,5/3 => mKết tủa = 27×0,5/3 = 4,5 gam.