Cho hai bình điện phân, bình (1) đựng 20 ml dung dịch NaOH 1,73M; bình (2) đựng dung dịch gồm 0,225 mol và 0,2 mol HCl. Mắc nối tiếp bình (1) và bình (2). Điện phân các dung dịch bằng dòng điện một chiều với cường độ dòng điện không đổi một thời gian. Khi dừng điện phân, tháo ngay catot ở các bình. Sau phản ứng thấy nồng độ NaOH ở bình (1) là 2M, Cho tiếp 14 gam bột Fe vào bình (2) đến khi phản ứng xảy ra hoàn toàn thu được m gam chất rắn không tan. Biết NO là sản phẩm khử duy nhất khối lượng riêng của nước là 1 g/ml. Giá trị m là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.




Đáp án C

- Sau điện phân:
+ Thể tích dung dịch NaOH ở bình 1 = 0 , 0692 2 =0,03461=34,6 ml
=> Thể tích nước bị điện phân = 40 - 34,6 = 5,4 ml
=> Số mol nước bị điện phân ở bình 1 = 5 , 4 18 = 0,3 mol
+ Bình 2:
n Cu = n H 2 O điện phân ( I ) = 0 , 3 mol ⇒ n Cu 2 + dư = 0 , 45 - 0 , 3 = 0 , 15 mol n Cl 2 = 1 2 n Cl - = 0 , 2 mol ⇒ n H 2 O điện phân ( 1 ) = 0 , 3 - 0 , 2 = 0 , 1 mol ⇒ n H + = 0 , 2 + 0 , 4 = 0 , 6 mol
- Cho 0,5 mol Fe vào dung dịch bình 2 sau phản ứng điện phân
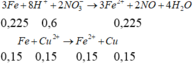
=> m = 56.(0,5-0,225-0,15)+64.0,15=16,6 gam gần với giá trị 17 nhất

Đáp án : C
Bình 1 : Chỉ có điện phân nước => nNaOH =const = 0,0346
=> Vdd sau = 17,3 ml => VH2O mất = 1,7 ml => mH2O = 2,7g
=> ne trao đổi = 0,15 mol . 2 = 0,3 mol = ne (bình 2)
(Vì mắc nối tiếp nên dòng điện cường độ không đổi)
Bình 2 :
Catot :
Cu2+ + 2e -> Cu
Anot :
2Cl- -> Cl2 + 2e
2H2O -> 4H+ + O2 + 4e
=> Sau phản ứng có 0,075 mol Cu2+ ; (0,2 + 0,1) mol H+ ; 0,45 mol NO3- có thể phản ứng với Fe
,nFe = 0,25 mol
3Fe + 8H+ + 2NO3- -> 3Fe2+ + 2NO + 4H2O
Fe + Cu2+ -> Fe2+ + Cu
=> Chất rắn gồm : 0,075 mol Cu và 0,0675 mol Fe
=> m = 8,3g

Giải thích: Đáp án C
+ Bình 1: nNaOH=0,0346 mol
Sau khi x mol H2O bị điện phân thì thể tích dung dịch còn lại là 20-18x (ml)
=> CM=0,0346/[(20-18x)/1000] = 2
=> x=0,15
=> ne = 2x = 0,3
Bình 2:
Tại catot:
Cu2+ +2e → Cu
0,15.....0,3
Cu2+ dư 0,225-0,15=0,075 mol
Tại anot:
Cl- -1e → 0,5 Cl2
0,2→0,2
H2O – 2e → 0,5O2 + 2H+
0,1 → 0,1
Dung dịch trong bình 2 sau điện phân gồm: 0,075 mol Cu2+; H+: 0,2+0,1=0,3 mol
Khi cho 0,25 mol Fe vào:
3Fe + 8H+ + 2NO3- → 3Fe2+ + 2NO + 4H2O
Bđ: 0,25 0,3 0,45
Pư: 0,1125← 0,3 →0,075
Sau: 0,1375
Fe + Cu2+ → Fe2+ + Cu
Bđ:0,1375 0,075
Pư:0,075 ← 0,075 →0,075
Sau:0,0625 0,075
=> m chất rắn = 0,0625.56+0,075.64=8,3 gam

Đáp án D
Ta có: mắc nối tiếp nên hai bình điện phân cùng I.
• bình 1: giải điện phân NaOH → có thể coi là quá trình điện phân H2O
từ CM (NaOH) → nH2O bị điện phân = 0,15 mol ⇄ ne trao đổi = 0,3 mol.
• dùng giả thiết ne trao đổi trên: có điện phân bình 2 ra: 0,1 mol CuCl2 + 0,05 mol CuO.
||→ bảo toàn gốc NO3 đọc ra dd sau điện phân gồm 0,075 mol Cu(NO3)2 và 0,3 mol HNO3.
Quy về giải 0,25 mol Fe + 0,075 mol Cu(NO3)2 + 0,3 mol HNO3 → ? gam chất rắn không tan.!
Giải: m gam chất rắn gồm 0,075 mol Cu và 0,0625 mol Fe ⇄ m = 8,3 gam.

Đáp án D
Ở đây có dùng một kiến thức vật lí: mắc nối tiếp nên hai bình điện phân cùng I
• bình (1): giải điện phân NaOH → có thể coi là quá trình điện phân H2O
từ CM (NaOH) → nH2O bị điện phân = 0,15 mol ⇄ ne trao đổi = 0,3 mol.
• dùng giả thiết ne trao đổi trên: có điện phân bình (2) ra: 0,1 mol CuCl2 + 0,05 mol CuO.
→ bảo toàn gốc NO3 đọc ra dd sau điện phân gồm 0,075 mol Cu(NO3)2 và 0,3 mol HNO3.
Quy về giải 0,25 mol Fe + 0,075 mol Cu(NO3)2 + 0,3 mol HNO3 → ? gam chất rắn không tan.!
Giải: m gam chất rắn gồm 0,075 mol Cu và 0,0625 mol Fe ⇄ m = 8,3 gam

Đáp án D
Ở đây có dùng một kiến thức vật lí:
mắc nối tiếp nên hai bình điện phân cùng I.
• bình (1): giải điện phân NaOH
→ có thể coi là quá trình điện phân H2O
từ CM (NaOH) → nH2O bị điện phân = 0,15 mol ⇄ ne trao đổi = 0,3 mol.
• dùng giả thiết ne trao đổi trên: có điện phân bình (2) ra:
0,1 mol CuCl2 + 0,05 mol CuO.
||→ bảo toàn gốc NO3 đọc ra dd sau điện phân gồm 0,075 mol Cu(NO3)2 và 0,3 mol HNO3.
Quy về giải 0,25 mol Fe + 0,075 mol Cu(NO3)2 + 0,3 mol HNO3
→ ? gam chất rắn không tan.!
Giải: m gam chất rắn gồm 0,075 mol Cu và 0,0625 mol Fe ⇄ m = 8,3 gam.

a) Gọi CTPT của Y là CxHyOz ( x, y, z € N*)
Đốt cháy Y sản phẩm thu được gồm H2O và CO2. Khi cho sản phẩm qua H2SO4 đặc dư thì H2O bị hấp thụ, tiếp tục cho qua KOH dư thì CO2 bị hấp thụ
=> mB1 tăng = mH2O = 0,72 (g) => nH2O = 0,72/18 = 0,04 (mol)
mB2 tăng = mCO2 = 3,96 (g) => nCO2 = 3,96/44 = 0,09 (mol)
BTKL: nO (trong A) = (mA – mC – mH )/16 = (1,48 – 0,09.12 – 0,04.2 )/16 = 0,02 (mol)
Ta có: x : y : z = nC : nH : nO
= 0,09 : 0,08 : 0,02
= 9 :8 : 2
CTPT trùng với CT ĐGN => CTPT củaY là: C9H8O2
Độ bất bão hòa của Y: C9H8O2: k = ( 9.2 + 2 – 8) /2 = 6
Y không tham gia phản ứng tráng bạc => Y không có cấu tạo nhóm – CHO trong phân tử
Y + KMnO4 → Y1 ( MY1 = MY + 34 ) => Y có chứa liên kết đôi C=C khi phản ứng với KMnO4 sẽ tạo thành C(OH)-C(OH)
nY = 1,48: 148 = 0,01 (mol) ; nNaOH = 0,02 (mol)
nY : nNaOH = 1: 2 và sản phẩm tạo thành 2 muối => Y là este của axit cacboxylic và phenol hoặc dẫn xuất của phenol
Vậy CTCT của Y thỏa mãn là: CH2=CH-COOC6H5: phenyl acrylat
3CH2=CH-COOC6H5 + 2KMnO4 + 4H2O → 3CH2(OH)-CH(OH)-COOC6H5 + 2MnO2↓ + 2KOH
b) Z là đồng phân của Y => Z có cùng CTPT là: C9H8O2
nZ = 0,37/148 = 0,025 (mol); nNaOH = 0,025 (mol); nAg = 0,01 (mol)
nZ : nNaOH = 1: 1 => Z có 1 trung tâm phản ứng với NaOH
Ta thấy nAg = 4nZ => Z phải phản ứng với NaOH sinh ra cả 2 chất hữu cơ đều có khả năng tham gia phản ứng tráng bạc ( mỗi chất tham gia phản ứng tráng bạc sinh ra 2Ag)
Z chỉ phản ứng với H2 ( Pb, t0) theo tỉ lệ 1: 1 => Z có 1 liên kết đôi C=C ngoài mạch
Vậy CTCT của Z thỏa mãn là: HCOOCH=CH-C6H5
HCOOCH=CH-C6H5 + NaOH → COONa + C6H5CH2CHO
HCOONa + 2AgNO3 + 3NH3 + H2O → NH4O-COONa + 2Ag ↓ + 2NH4NO3
C6H5CH2CHO + 2AgNO3 + 3NH3 + H2O → C6H5CH2COONH4+ 2Ag↓ + 2NH4NO3

