Đem nung hỗn hợp hai oxit CuO và ZnO có tỉ lệ số mol là 1 : 1 với cacbon trong điều kiện thích hợp để oxit kim loại bị khử hết, thu được hỗn hợp chất rắn X. Cho X tác dụng với dung dịch HCl dư thấy thoát ra 2,24 lít khí (ở đktc). Hãy tính khối lượng mỗi oxit kim loạ
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


2.
Khí thoát ra là khí \(H_2:n_{H2}=0,2\left(mol\right)\)
\(\rightarrow n_M=0,2\left(mol\right)\)
CuSO4 chỉ tác dụng với M \(\rightarrow n_{CuSO4_{pu}}=0,2\left(mol\right)\)
Trong 62g chất rắn có CuSO4 dư và MSO4
\(\rightarrow m_{MSO4}=62-0,2.160=30\left(g\right)\)
\(m_{MSO4}=14,8+96.0,1-m_{MO}=30g\rightarrow m_{MO}=4g\)
Bảo toàn khối lượng : mhh =mM + mMO + mMSO4
\(14,8=0,2M+4+\left\{30-\left[0,2.\left(M+96\right)\right]\right\}\)
\(\rightarrow M=24\left(Mg\right)\)\(\rightarrow\%m_M=32,43\%,\%m_{MO}=27,03\%,\%m_{SO4}=40,54\%\)
1.
\(nH_2\) để khử oxit \(=0,09\left(mol\right)\)
\(A_2O_x+xH_2\rightarrow2A+xH_2O\left(1\right)\)
\(CuO+H_2\rightarrow Cu+H_2O\left(2\right)\)
Do Cu không tác dụng với hcl nên chỉ có kim loại a sinh ra pư với HCl sinh ra khí H2
\(nH_{2_{sinh.ra}}=0,06\left(mol\right)\)
Gọi hóa trị củaA là x
\(2A+2xHCl\rightarrow2AClx+xH_2\left(3\right)\)
0,12/x__________________0,06
Giả sử hoá trị của A không đổi trong oxit và trong muối ( trừ trường hợp của \(Fe_2O_3\)) nên \(NH_2\left(1\right)=NH_2\left(3\right)\)
\(n_{CuO}=n_{H2}=0,09-0,02=0,03\)
\(n_A=0,03.6=1,2\rightarrow n_{A2Ox}=0,06\)
\(2A+16x=\frac{5,44-0,03.80}{0,06}=50,666\left(loai\right)\)
Vậy giả sử oxit là \(Fe_2O_3\)

Gọi oxit kim loại phải tìm là MO và nCuO = a và nMO =2a
nHNO3 = 0.15 mol
Vì hiđro chỉ khử được những oxit kim loại đứng sau nhôm trong dãy điện hóa nên có 2 trường hợp xảy ra.
∙ Trường hợp 1: M đứng sau nhôm trong dãy điện hóa
CuO + H2 → Cu + H2O
MO + H2 → M + H2O
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
3M + 8HNO3 → 3M(NO3)2 + 2NO + 4H2O
Ta có hệ pt:
{ 80a + (M +16).2a = 3.6
8a/3 + 16a/3 = 0.15 }
a = 0,01875 và M = 40 → M là Ca.
Trường hợp này loại vì CaO không bị khử bởi khí H2.
∙ Trường hợp 2: M đứng trước nhôm trong dãy điện hóa
CuO + H2 → Cu + H2O
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
MO + 2HNO3 → M(NO3)2 + 2H2O
Ta có hệ pt:
{ 80a + (M +16).2a = 3.6
8a/3 + 4a = 0.15 }
a = 0,0225 và M = 24 → M là Mg → Đáp án C

Đáp án C
Gọi số mol CuO và MO là a,2a(mol)
TH1:CO khử được MO
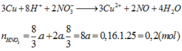
=>a=0,025=>80a+(M+16).2a=4,8
=>M là Ca(loại vì CaO không bị CO khử)
Không có M thỏa mãn lọai
TH2.CO không khử đc MO
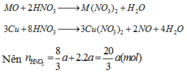
=>a=0,03(mol) =>80a+(M+16).2a=4,8=>M=24

Đáp án C
Gọi số mol CuO và MO là a,2a(mol)
TH1:CO khử được MO
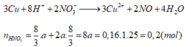
=>a=0,025=>80a+(M+16).2a=4,8=>M là Ca(loại vì CaO không bị CO khử)
Không có M thỏa mãn lọai
TH2.CO không khử đc MO
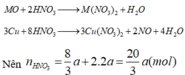
=>a=0,03(mol) =>80a+(M+16).2a=4,8=>M=24

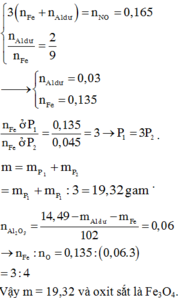


Sơ đồ phản ứng: ZnO, CuO → C Zn, Cu
Zn + 2HCl → Zn Cl 2 + H 2
n H 2 = 2,24/22,4 = 0,1 mol
n Zn = 0,1 mol
Theo đề bài, ZnO, CuO có tỷ lệ số mol là 1:1 nên Zn và Cu cũng có tỉ lệ số mol 1:1
=> n Cu = n Zn = 0,1 mol
m CuO = 8g; m ZnO = 8,1g