Đốt cháy hoàn toàn hỗn hợp X gồm tinh bột, xenlulozơ và glucozơ cần vừa đủ 3,36 lít O2 (đktc), thu được 2,34 gam nước. Phần trăm khối lượng của glucozơ trong X là
A. 21,74%.
B. 18,37%.
C. 20,00%.
D. 16,67%.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

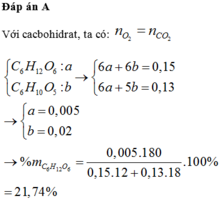

Chọn A
Có CTPT của axit axetic là C2H4O2; glucozơ là C6H12O6; saccarozơ C12H22O11; xenlulozơ và tinh bột là (C6H10O5)n Þ Có thể quy đổi thành C và H2O Þ Xem như chỉ có phản ứng C + O2à CO2
Þ nC = nO2 = 0,54 Þ mM = 0,54x12 + 0,49x18 = 15,3 gam.

Đốt cháy hỗn hợp gồm các cacbohiđrat thu được số mol CO2 bằng số mol O2 cần dùng vừa đủ (0,75 mol), số mol nước thu được là 0,65 mol.
Khối lượng hỗn hợp X là 0,75.44+0,65.18 -0,75.32 = 20,7 (g).
Gọi tổng số mol tinh bột và xenlulozơ ((C6H10O5)n) là x mol, số mol saccarozơ (C12H22O11) là y mol. Ta có:
\(\left\{{}\begin{matrix}6nx+12y=0,75\\5nx+11y=0,65\end{matrix}\right.\) ⇒ \(\left\{{}\begin{matrix}x=\dfrac{0,075}{n}\\y=0,025\end{matrix}\right.\).
Khối lượng của tinh bột trong X có giá trị từ trên 0 gam đến dưới 0,075/n.162n = 12,15 gam. Phần trăm khối lượng của tinh bột trong X có giá trị trong khoảng từ trên 0% đến gần bằng 58,70%.

Đáp án A
Gọi công thức chung của chúng là Cn(H2O)m
Khi đốt cháy ta có: Cn(H2O)m+nO2→nCO2+mH2O
nCO2=nO2 = 0,1125 mol
Áp dụng định luật bảo toàn khối lượng:
m = 0,1125.44 + 1,8 – 0,1125.32 = 3,15 gam

Đáp án D
4 chất Xenlulozơ , tinh bột, fructozơ, glucozơ, đều thuộc cacbohi đrat => CTTQ: Cn(H2O)m
Bản chất đốt cháy các chất này là quá trình đốt cháy Cacbon:![]()
Từ PTHH: => nC = nO2 = 2,52 : 22,4 = 0,1125 (mol)
BTKL: m = mC + mH2O = 0,1125. 12 + 1,8 = 3,15 (g)